题目内容
(2008?南岗区一模)张南同学取来某种品牌的胃药30g放入烧杯中,再加入82g的稀盐酸,充分反应后所得混合物的质量为103.2g,此时溶液的pH为7.若此胃药中只含氢氧化铝、氧化镁、碳酸氢钠等常见的治疗胃病药剂中的一种.且胃药中的其他成分不与盐酸反应也不溶于水.试回答:(1)此胃药中含有的治疗胃病药剂是______
(2)发生反应的化学方程式是______
(3)列出参加反应的药剂质量(x)的比例式为______
(4)反应后所得溶液溶质的质量分数是______.
【答案】分析:理解酸的化学性质及能够和酸反应的常见的物质,并能进行简单的有关的计算.
解答:解:(1)30克胃药与80克盐酸混合,充分反应后只得到103.2克混合物,少了8.8克,说明生成了8.8气体,由于在氢氧化铝、氧化镁、碳酸氢钠,只有碳酸氢钠与盐酸反应能生成气体.故答案为:碳酸氢钠
(2)由于碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,故答案为:NaHCO3+HCl=NaCl+H2O+CO2↑
(3)该题的具体过程为:设参加反应的药剂即碳酸氢钠的质量为X,生成的氯化钠的质量为Y.
NaHCO3+HCl=NaCl+H2O+CO2↑
84 58.5 44
X Y 8.8

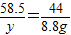
x= =16.8g y=
=16.8g y= =11.7g
=11.7g
所的溶液中溶质的质量分数为: ×100%═13%
×100%═13%
故答案为:
(4)13%
点评:主要考查了酸的化学性质,常见化学方程式的书写,培养学生分析问题、解决问题、计算的能力.
解答:解:(1)30克胃药与80克盐酸混合,充分反应后只得到103.2克混合物,少了8.8克,说明生成了8.8气体,由于在氢氧化铝、氧化镁、碳酸氢钠,只有碳酸氢钠与盐酸反应能生成气体.故答案为:碳酸氢钠
(2)由于碳酸氢钠与稀盐酸反应生成氯化钠、二氧化碳和水,故答案为:NaHCO3+HCl=NaCl+H2O+CO2↑
(3)该题的具体过程为:设参加反应的药剂即碳酸氢钠的质量为X,生成的氯化钠的质量为Y.
NaHCO3+HCl=NaCl+H2O+CO2↑
84 58.5 44
X Y 8.8

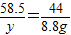
x=
 =16.8g y=
=16.8g y= =11.7g
=11.7g所的溶液中溶质的质量分数为:
 ×100%═13%
×100%═13%故答案为:

(4)13%
点评:主要考查了酸的化学性质,常见化学方程式的书写,培养学生分析问题、解决问题、计算的能力.

练习册系列答案
相关题目
(2008?南岗区一模)实验窒里区分下列物质的两个实验设计方案都合理的是( )
| A | B | C | D | |
| 区分物质 | 聚乙烯(PE)和聚氯乙烯(PVC) | 铁粉和碳粉 | 羊毛纤维和涤沦纤维 | (NH4)2SO4和NH4NO3 |
| 第一方案 | 观察颜色 | 用磁铁 | 观察颜色 | 加碱后,加热,闻气味 |
| 第二方案 | 取样分别点燃,闻燃烧时的气味 | 在空气中点燃,观察燃烧情况 | 闻燃烧产生气味,观察燃烧情况和灰烬 | 加硝酸钡溶液,观察是否有沉淀 |
