题目内容
这里有一杯盐水(NaCl和H2O的混合物)总质量共80克,其中NaCl的质量为11.7克,水的质量为68.3g.(1)这杯盐水中氯化钠的质量分数为______(保留到小数点后一位)
(2)计算NaCl中的钠元素的质量分数为______(保留到小数点后一位)
(3)计算这杯盐水中含钠元素的质量为______
(4)计算这杯盐水中钠元素的质量分数为______.
【答案】分析:根据溶质质量分数公式以及化学式的计算公式进行,已知溶质的质量和溶液的质量,根据公式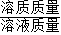 ×100%即可求得溶质质量分数,要求氯化钠中钠元素的质量分数,根据公式
×100%即可求得溶质质量分数,要求氯化钠中钠元素的质量分数,根据公式 ×100%即可求得.
×100%即可求得.
解答:解:(1)氯化钠的质量分数: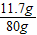 ×100%=14.6%所以本题答案为:14.6%,
×100%=14.6%所以本题答案为:14.6%,
(2)NaCl中的钠元素的质量分数: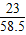 ×100%=39.3%,所以本题答案为:39.3%,
×100%=39.3%,所以本题答案为:39.3%,
(3)钠元素的质量为:11.7g×39.3%=4.6g,所以本题答案为:4.6g,
(4)这杯盐水中钠元素的质量分数为: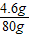 ×100%=5.75%,所以本题答案为:5.75%.
×100%=5.75%,所以本题答案为:5.75%.
点评:本题考查了有关溶质质量分数以及根据化学式的有关计算,完成此题,可以依据溶质质量分数公式以及根据化学式的计算公式进行.
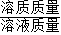 ×100%即可求得溶质质量分数,要求氯化钠中钠元素的质量分数,根据公式
×100%即可求得溶质质量分数,要求氯化钠中钠元素的质量分数,根据公式 ×100%即可求得.
×100%即可求得.解答:解:(1)氯化钠的质量分数:
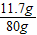 ×100%=14.6%所以本题答案为:14.6%,
×100%=14.6%所以本题答案为:14.6%,(2)NaCl中的钠元素的质量分数:
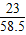 ×100%=39.3%,所以本题答案为:39.3%,
×100%=39.3%,所以本题答案为:39.3%,(3)钠元素的质量为:11.7g×39.3%=4.6g,所以本题答案为:4.6g,
(4)这杯盐水中钠元素的质量分数为:
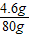 ×100%=5.75%,所以本题答案为:5.75%.
×100%=5.75%,所以本题答案为:5.75%.点评:本题考查了有关溶质质量分数以及根据化学式的有关计算,完成此题,可以依据溶质质量分数公式以及根据化学式的计算公式进行.

练习册系列答案
相关题目