题目内容
 我国某地区有一种“冬天捞碱,夏天晒盐”的说法,这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中含有少量NaCl.某化学课外活动小组为了解释捞碱、晒盐的原理和测定“碱”样品中Na2CO3的含量进行了以下探究.
我国某地区有一种“冬天捞碱,夏天晒盐”的说法,这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中含有少量NaCl.某化学课外活动小组为了解释捞碱、晒盐的原理和测定“碱”样品中Na2CO3的含量进行了以下探究.【查阅资料】
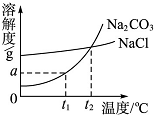
Na2CO3和NaCl的溶解度曲线如图所示.
(1)根据图示回答:①t1℃时Na2CO3的溶解度为
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度的降低而
③“夏天晒盐”是利用
A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl的溶解度增大
【实验步骤】
第一步:称取34.6g“碱”样品.
第二步:将该样品放入130g稀盐酸中,两者恰好完全反应.其化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑
第三步:完全反应后,称得溶液的总质量为151.4g,经计算可知释放出的二氧化碳的质量为13.2g.
【数据分析】
(2)试计算:(结果保留一位小数)
①Na2CO3的相对分子质量.
②34.6g“碱”样品中碳酸钠的质量.
③“碱”样品中Na2CO3的纯度.
【继续探究】
(3)计算反应后所得溶液中NaCl的质量分数.
练习册系列答案
相关题目
下列微观粒子结构示意图的相关叙述正确的是( )
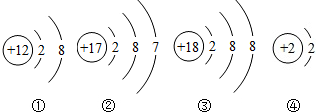

| A、①②③的原子的电子层数相同 | B、①③的元素在周期表的同一族 | C、只有①③具有相对稳定结构 | D、②易得电子,④易失电子 |
下列化学实验基本操作图示正确的是( )
A、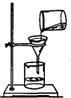 过滤 | B、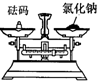 称取氯化钠 | C、 稀释浓硫酸 | D、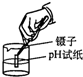 测溶液pH |
下列关于海水晒盐原理的分析,正确的是( )
| A、利用阳光和风力将水分蒸发得到食盐 | B、利用机械动力搅拌得到食盐 | C、利用阳光照射使海水升温得到食盐 | D、利用海水在阳光下发生分解反应制得食盐 |
下列实验操作中,正确的是( )
A、 蒸发食盐水 | B、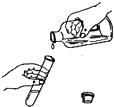 倾倒液体 | C、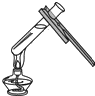 加热液体 | D、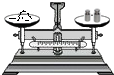 称量固体 |
下列图示实验操作中,不正确的是( )
A、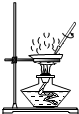 蒸发 | B、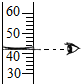 读取液体体积 | C、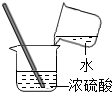 稀释浓硫酸 | D、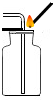 证明CO2是否集满 |
下列对自然界中的水进行净化处理的方法中,净化程度最高的方法是( )
| A、蒸馏 | B、沉降 | C、过滤 | D、吸附 |
水是重要的资源,我们需要了解水、认识水.下列说法错误的是( )
| A、肥皂水能区分硬水和软水 | B、海水中加入明矾可以使其变成淡水 | C、利用吸附、沉淀、过滤和蒸馏等方法可以净化水 | D、电解水时加入氢氧化钠,是为了电解水时产生更多的氢气和氧气 |
