|
|
强电解质 |
弱电解质 |
|
定义 |
溶于水后几乎完全电离的电解质 |
溶于水后只有部分电离的电解质 |
|
化合物类型 |
离子化合物及具有强极性键的 共价化合物 |
某些具有弱极性键的共价化合物。 |
|
电离程度 |
几乎100%完全电离 |
只有部分电离 |
|
电离过程 |
不可逆过程,无电离平衡 |
可逆过程,存在电离平衡 |
|
溶液中存在的微粒(水分子不计) |
只有电离出的阴阳离子,不存在 电解质分子 |
既有电离出的阴阳离子,又有电解质分子 |
|
实例 |
绝大多数的盐(包括难溶性盐) 强酸:H2SO4、HCl、HClO4等 强碱:Ba(HO)2 Ca(HO)2等 |
弱酸:H2CO3
、CH3COOH等。 弱碱:NH3·H2O、Cu(OH)2 Fe(OH)3等。 |
|
电离方程式 |
KNO3=K++NO3- H2SO4=2 H++SO42- |
NH3·H2O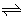 NH4++OH_ NH4++OH_H2S 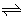 H++HS_ HS_ H++HS_ HS_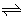 H++S2- H++S2- |
2.类型及其环节、作用
|
水循环类型 |
发生领域 |
水循环环节 |
作用 |
|
海陆间大循环 |
海洋与陆地之间 |
蒸发、水汽输送、凝结降水、地表径流、下渗、地下径流 |
使陆地水不断得到补充,水资源得以再生,是最重要的水循环,又称大循环 |
|
陆地内循环 |
陆地与陆地上空之间 |
蒸发、植物蒸腾、凝结降水等 |
补给陆地水体的水量为数很少 |
|
海上内循环 |
海洋与海洋上空之间 |
蒸发、凝结、降水等 |
水循环的水量最大,对于全球的热量输送有着重要意义 |
读图P59 水循环示意图
水循环在水圈、大气圈、岩石圈、岩石圈、生物圈四大圈层中通过蒸发、蒸发、植物蒸腾、水汽输送、降水、地表径流、下渗、地下径流等环节连续运动。它发生的领域有:海洋与陆地之间,陆地与陆地上空之间,海洋与海洋上空之间。
从图中还可以看出:
水循环的基本环节有三个:①降水,包括陆地降水和海上降水;②蒸发,包括海上蒸发、陆面蒸发、植物蒸腾;③输送,包括水汽输送和径流输送。
水循环的组成,分为两部分:即大气部分--水汽输送阶段和降水阶段;地面部分--径流阶段与蒸发阶段。每一部分都包含三个方面,即水分输送、暂时储存和状态的变化。关于状态的变化,在大气部分是通过凝结,把气态转变成液态,地面部分是通过蒸发,把液态转变成气态。
水循环把自然界的各部分联系起来,形成一个有机整体。在垂直方向上,通过降水、蒸发、下渗、植物蒸腾等环节,把大气圈、水圈、生物圈、岩石圈联系起来;通过水汽输送的径流输送,把陆地和海洋联系起来。这样就构成一个庞大的水循环系统。
注意:海陆间循环又称为大循环是指该循环环节最多(包括海洋水蒸发、水汽输送、凝结降水、地表径流、下渗、地下径流等)、范围最广(既包括海洋也包括陆地)。而不是指参与的水量,就水循环参与的水量而言,海上内循环是海陆间循环的9倍。
1.水圈的概念和特点
水在地理环境中以气态、固态和液态三种形式相互转化,形成各种水体,共同构成了一个连续但不规则的圈层。
组成水圈的液态水、气态水、固态水的分布和数量特征可用表格形式比较如下:
|
水的三态 |
分布特点 |
数量特征 |
|
气态水 |
最广 |
最少 |
|
液态水 |
次之 |
最大 |
|
固态水 |
仅在高纬、高山或特殊条件下才能存在 |
地球淡水的主体,水量约占淡水总量的2/3 |
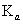 表示,碱用
表示,碱用 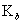 表示)。
表示)。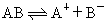
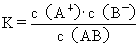
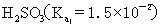 >
> 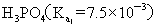 >
> 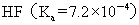 >
> 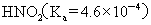 >
> 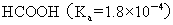 >
> 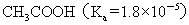 >
> 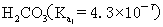 >
> 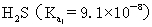
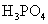 的电离:
的电离: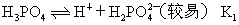
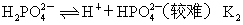
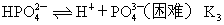
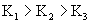 。在磷酸溶液中,由
。在磷酸溶液中,由 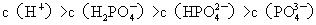 。
。

 大气降水 降雨 江河水
融水 冰川
大气降水 降雨 江河水
融水 冰川

 下渗 下渗
下渗 下渗

 地下水
地下水