摘要:24.氯化钠既是重要的调味品.又是重要的工业原料. ①实验室里有一小袋粗盐.其中含有较多的可溶性杂质(MgCl2.CaCl2等)和泥沙等不溶性杂质.要初步提纯这袋粗盐需要经过的步骤是溶解.过滤和 .若要计算提纯后所得精盐的产率.必须用的仪器是 . ②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气.氯气.化学方程式为: .
网址:http://m.1010jiajiao.com/timu_id_920620[举报]
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和 .若要计算提纯后所得精盐的产率.必须用的仪器是 .
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
2R+H2↑+Cl2↑,其中R的化学式为 ,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为 g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
| ||
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
| ||
氯化钠既是重要的调味品,又是重要的工业原料.
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O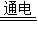 2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
查看习题详情和答案>>
①实验室里有一小袋粗盐,其中含有较多的可溶性杂质(MgCl2、CaCl2等)和泥沙等不溶性杂质,要初步提纯这袋粗盐需要经过的步骤是溶解、过滤和______.若要计算提纯后所得精盐的产率.必须用的仪器是______.
②工业上用给饱和食盐水通电的方法可制得一种碱R和氢气、氯气,化学方程式为:
2NaCl+2H2O
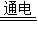 2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.
2R+H2↑+Cl2↑,其中R的化学式为______,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为______g.查看习题详情和答案>>
 2R+H2↑+Cl2↑,其中R的化学式为________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为________g.
2R+H2↑+Cl2↑,其中R的化学式为________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为________g. 2R+H2↑+Cl2↑,其中R的化学式为__________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为___g。
2R+H2↑+Cl2↑,其中R的化学式为__________,若反应中消耗了58.5g氯化钠,则理论上可得到R的质量为___g。