摘要:27.某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应.从不同角度设计了如下实验方案.并进行实验.方案一:先用pH试纸测定氢氧化钠溶液的pH.再滴加盐酸.并不断振荡溶液.同时测定混合溶液的pH.如果测得的pH逐渐变小且小于7.则证明氢氧化钠溶液与稀盐酸发生了化学反应.(1)用pH试纸测定溶液的pH时.正确的操作是: .(2)简述强调“测得的pH小于7 的理由 .方案二:先在氢氧化钠溶液中滴加几滴酚酞试液.溶液显红色.然后再滴加盐酸.可观察到红色逐渐消失.则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时.发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液.溶液逐渐变成了红色.过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应.使红色消失,②可能是酚酞试液与空气中的二氧化碳反应.使红色消失.(1)为验证猜想①.该组同学做了如下实验:将配制的氢氧化钠溶液加热.并在液面上方滴一些植物油.然后在冷却后的溶液中滴人酚酞试液.实验中“加热 的目的是 .“滴入植物油 的目的是 .实验结果证明酚酞试液红色消失与空气中的氧气无关.(2)为验证猜想②.该组同学做了如下实验:取一定量的碳酸钠溶液.在其中滴入酚酞试液.发现溶液也呈红色.由此可以得出以下两个结论:结论1:说明 ,结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时.就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:①实验方法 ,②观察到的现象 .方案三:化学反应中通常伴随能量的变化.可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合.用温度计测定室温下混合前后溶液温度的变化.并记录了每次混合前后温度的升高值△t.
网址:http://m.1010jiajiao.com/timu_id_918492[举报]
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
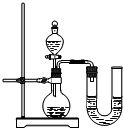
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.
 查看习题详情和答案>>
查看习题详情和答案>>
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
(1)表中X=______.
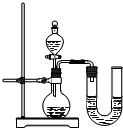
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.
查看习题详情和答案>>
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.

某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应。
(1)用pH试纸测定溶液的pH时,正确的操作是:______________________。
(2)简述强调“测得的pH小于7”的理由______________________________。
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应。该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了。该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失。
(3)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液。实验中“加热”的目的是____________________,“滴入植物油”的目的是____________________。实验结果证明酚酞试液红色消失与空气中的氧气无关。
(4)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈 性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关。
(5)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法__________________________________________________;
②观察到的现象______________________________________________。
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生。该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应。
(1)用pH试纸测定溶液的pH时,正确的操作是:______________________。
(2)简述强调“测得的pH小于7”的理由______________________________。
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应。该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了。该小组同学对这种意外现象的原因做了如下猜想:
①可能是酚酞试液与空气中的氧气反应,使红色消失;
②可能是酚酞试液与空气中的二氧化碳反应,使红色消失。
(3)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞试液。实验中“加热”的目的是____________________,“滴入植物油”的目的是____________________。实验结果证明酚酞试液红色消失与空气中的氧气无关。
(4)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明碳酸钠溶液呈 性;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关。
(5)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法__________________________________________________;
②观察到的现象______________________________________________。
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生。该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
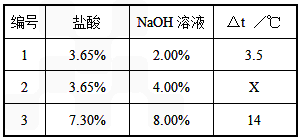

(6)表中X=__________。
(7)某同学在没使用温度计的情况下,通过上图所示装置完成了实验。该同学根据___________________________判断氢氧化钠溶液与稀盐酸发生了中和反应。
查看习题详情和答案>>
(7)某同学在没使用温度计的情况下,通过上图所示装置完成了实验。该同学根据___________________________判断氢氧化钠溶液与稀盐酸发生了中和反应。
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
(1)表中X=______.
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.
查看习题详情和答案>>
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.

查看习题详情和答案>>
某兴趣小组为证明氢氧化钠溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
(1)表中X=______.
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.
查看习题详情和答案>>
方案一:先用pH试纸测定氢氧化钠溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明氢氧化钠溶液与稀盐酸发生了化学反应.
(1)用pH试纸测定溶液的pH时,正确的操作是:______.
(2)简述强调“测得的pH小于7”的理由______.
方案二:先在氢氧化钠溶液中滴加几滴酚酞试液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明氢氧化钠溶液与稀盐酸发生了化学反应.该组同学在向氢氧化钠溶液中滴加酚酞试液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞试液,溶液逐渐变成了红色,过了一会儿红色就消失了.该小组同学对这种意外现象的原因做了如下猜想:①可能是酚酞试液与空气中的氧气反应,使红色消失;②可能是酚酞试液与空气中的二氧化碳反应,使红色消失.
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴人酚酞试液.实验中“加热”的目的是______,“滴入植物油”的目的是______.实验结果证明酚酞试液红色消失与空气中的氧气无关.
(2)为验证猜想②,该组同学做了如下实验:取一定量的碳酸钠溶液,在其中滴入酚酞试液,发现溶液也呈红色,由此可以得出以下两个结论:
结论1:说明______;
结论2:说明酚酞试液红色消失与空气中的二氧化碳无关.
(3)该小组同学通过查阅资料得知:.当氢氧化钠溶液浓度很大时,就会出现上述意外现象.请设计实验证明该方案中取用的氢氧化钠溶液浓度过大:
①实验方法______;
②观察到的现象______.
方案三:化学反应中通常伴随能量的变化,可借助反应前后温度的变化判断反应的发生.该组同学将不同浓度的盐酸和氢氧化钠溶液各10mL混合,用温度计测定室温下混合前后溶液温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
(2)某同学在没使用温度计的情况下,通过上图所示装置完成了实验.该同学根据______判断氢氧化钠溶液与稀盐酸发生了中和反应.

查看习题详情和答案>>