摘要:1.目前.下列化学制品在生活中不准使用的是 A.含磷洗衣粉 B.可降解塑料袋 C.高效低毒蚊香 D.合成纤维衣服
网址:http://m.1010jiajiao.com/timu_id_914519[举报]
I:牙膏是人们生活中的必需品,在牙膏的生产中常添加一种摩擦剂.这种摩擦剂是由某种自然界中分布很广的矿石A,经过一系列加工而制得的极细小的轻质碳酸钙粉末,其生产过程如下:
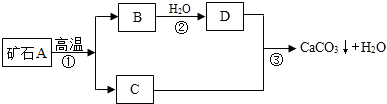
试回答:
(1)写出 C、D两种物质的化学式 C
(2)写出③反应的化学方程式
(3)反应③制轻质碳酸钙粉末后,还要通过
II、某兴趣小组为了测定本地所产矿石A的纯度,利用下图装置设计了以下实验方案:
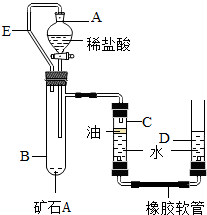 【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.
【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.
【实验步骤】
①连接装置并检查装置气密性;
②在试管B中加入10克矿石A,分液漏斗中加入足量的稀盐酸,C、D管中加入一定量的水,C管的液面上加一 层油,并将分液漏斗A和试管B用长导管E连接起来.
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加稀盐酸至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中B液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥计算气体的质量并由此求出矿石A中碳酸钙的质量分数
【实验分析】
(1)小明同学认为在实验前要将矿石A 全磨成粉末状,你认为他的目的是:
(2)小洁同学认为该实验的设计中最经典的是连接仪器A和仪器B的橡胶管E,你认为如果没有橡胶管E,则会对实验结果产生何种影响?
(3)检查该装置的气密性时,如图准备好装置,在C、D两管中装好水且液面相平,提高D管,
(4)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验:清判断并说明理由
(5)实验结束时同学们才发现由于粗心,小伟将植物油加到了D管的水面上,大家一致认为由于该粗心将会导致测得的矿石A中碳酸钙的质量分数产生误差,你认为该误差是
(6)化学老师看了他们的实验设计后,对他们的设计方案和合作意识、探究精神都给予了很高的评价,并对他们进行启发:二氧化碳的质量可以根据质量守恒定律,测反应前后烧杯中剩余物质的质量之差来求得,于是他们又在烧杯中进行了如下的实验测定:
请你和他们一起完成实验数记的分析和计算:
①当所取矿石A和稀盐酸的质量比
②矿石A中碳酸钙的质量分数是多少?
③所用稀盐酸的溶质质量分数是多少?
查看习题详情和答案>>

试回答:
(1)写出 C、D两种物质的化学式 C
CO2
CO2
DCa(OH)2
Ca(OH)2
(2)写出③反应的化学方程式
CO2+Ca(OH)2═CaCO3↓+H20
CO2+Ca(OH)2═CaCO3↓+H20
(3)反应③制轻质碳酸钙粉末后,还要通过
过滤
过滤
(填操作)将其从反应后的混合物中分离出来.实验室进行该操作时主要用到的玻璃仪器有:烧杯、玻璃棒、漏斗
漏斗
.II、某兴趣小组为了测定本地所产矿石A的纯度,利用下图装置设计了以下实验方案:
 【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.
【实验原理】:测定一定质量的矿石A与足量稀盐酸反应产生的二氧化碳在常温常压下的体积,根据密度求出二氧化碳的质量,然后根据发生的化学反应方程式算出矿石A中碳酸钙的质量,进而求出矿石A中碳酸钙的质量分数.【实验步骤】
①连接装置并检查装置气密性;
②在试管B中加入10克矿石A,分液漏斗中加入足量的稀盐酸,C、D管中加入一定量的水,C管的液面上加一 层油,并将分液漏斗A和试管B用长导管E连接起来.
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加稀盐酸至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中B液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥计算气体的质量并由此求出矿石A中碳酸钙的质量分数
【实验分析】
(1)小明同学认为在实验前要将矿石A 全磨成粉末状,你认为他的目的是:
使矿石A中的碳酸钙能被稀盐酸充分反应完
使矿石A中的碳酸钙能被稀盐酸充分反应完
;(2)小洁同学认为该实验的设计中最经典的是连接仪器A和仪器B的橡胶管E,你认为如果没有橡胶管E,则会对实验结果产生何种影响?
滴加的稀盐酸会将试管B中空气排入C管中,使测得的二氧化碳的体积偏大.
滴加的稀盐酸会将试管B中空气排入C管中,使测得的二氧化碳的体积偏大.
(3)检查该装置的气密性时,如图准备好装置,在C、D两管中装好水且液面相平,提高D管,
C、D管之间能产生稳定的液面差
C、D管之间能产生稳定的液面差
,则气密性良好;(4)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验:清判断并说明理由
重新实验,因为中途加酸,装置中的气体会逸出.
重新实验,因为中途加酸,装置中的气体会逸出.
.(5)实验结束时同学们才发现由于粗心,小伟将植物油加到了D管的水面上,大家一致认为由于该粗心将会导致测得的矿石A中碳酸钙的质量分数产生误差,你认为该误差是
偏小
偏小
(填偏大或偏小).(6)化学老师看了他们的实验设计后,对他们的设计方案和合作意识、探究精神都给予了很高的评价,并对他们进行启发:二氧化碳的质量可以根据质量守恒定律,测反应前后烧杯中剩余物质的质量之差来求得,于是他们又在烧杯中进行了如下的实验测定:
| 实验次数 项目 |
第一次 | 第二次 | 第三次 |
| 所取矿石A的质量/g | 12 | 12 | 15 |
| 所加稀盐酸的质量/g | 120 | 150 | 100 |
| 剩余物质的质量 | 127.6 | 157.6 | 110.6 |
①当所取矿石A和稀盐酸的质量比
3:25
3:25
时,矿石A和稀盐酸恰好完全反应.②矿石A中碳酸钙的质量分数是多少?
③所用稀盐酸的溶质质量分数是多少?
(2013?泰安)小亮同学想通过实验探究某企业采用的氨碱法制的纯碱样品的成分及含量.
提出问题:该纯碱样品中含有哪些物质?
猜想与假设:通过分析,小亮做出如下假设:
(1)只含有Na2CO3;
(2)含有Na2CO3和NaHCO3
查阅资料:
(1)表中的现象Ⅰ为
(2)现象Ⅱ对应的化学方程式为
实验探究:为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
实验反思:
实验步骤①中,氯化钙溶液过量的目的是
提出问题2:如何测量该纯碱样品中各物质的含量?
(1)为测量该纯碱样品各成分的含量,小亮设计了:图(1)装置,通过称量B装置得到质量变化来确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①
②
(2)小亮在老师的指导下重新设计了如图(2)的实验装置.该实验有以下操作步骤: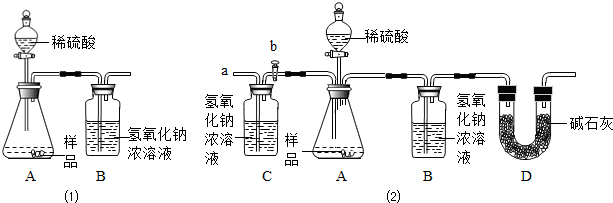
①检查装置气密性,将w g 干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是
查看习题详情和答案>>
提出问题:该纯碱样品中含有哪些物质?
猜想与假设:通过分析,小亮做出如下假设:
(1)只含有Na2CO3;
(2)含有Na2CO3和NaHCO3
查阅资料:
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
产生气泡
产生气泡
;(2)现象Ⅱ对应的化学方程式为
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
.实验探究:为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液. | 有白色沉淀产生 有白色沉淀产生 ; |
该反应的方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl Na2CO3+CaCl2═CaCO3↓+2NaCl . |
| ②将上述反应后的混合液过滤,取滤液 滴加稀盐酸 滴加稀盐酸 . |
有气泡冒出 有气泡冒出 ; |
证明猜想②成立. |
实验步骤①中,氯化钙溶液过量的目的是
将碳酸钠全部除去
将碳酸钠全部除去
.提出问题2:如何测量该纯碱样品中各物质的含量?
(1)为测量该纯碱样品各成分的含量,小亮设计了:图(1)装置,通过称量B装置得到质量变化来确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①
反应前装置A中含有空气,空气中含有二氧化碳,空气中的二氧化碳被吸收而使测量结果不准确
反应前装置A中含有空气,空气中含有二氧化碳,空气中的二氧化碳被吸收而使测量结果不准确
;②
反应后生成的二氧化碳不能全部被吸收,也会使测量结果不准确
反应后生成的二氧化碳不能全部被吸收,也会使测量结果不准确
.(2)小亮在老师的指导下重新设计了如图(2)的实验装置.该实验有以下操作步骤:

①检查装置气密性,将w g 干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是
①③②④⑥⑤⑦
①③②④⑥⑤⑦
.(2012?通州区一模)化学与生活息息相关,我们的衣食住行都离不开化学.
(1)生活中下列做法不正确的是
A.用灼烧的方法区分羊毛和涤纶 B.用活性炭使硬水软化
C.用观察的方法区分磷矿粉和尿素 D.用钢丝球擦洗铝锅
(2)目前一种叫碘酸钙[Ca(IO3)2]的保健品已进入一些超市,其中含有人体必需的微量元素是
(3)打开食醋的瓶盖,会闻到一股酸味,说明分子具有的性质是
(4)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.乙醇与汽油均属于
查看习题详情和答案>>
(1)生活中下列做法不正确的是
BD
BD
.A.用灼烧的方法区分羊毛和涤纶 B.用活性炭使硬水软化
C.用观察的方法区分磷矿粉和尿素 D.用钢丝球擦洗铝锅
(2)目前一种叫碘酸钙[Ca(IO3)2]的保健品已进入一些超市,其中含有人体必需的微量元素是
碘
碘
;Ca(IO3)2中I的化合价为+5
+5
.(3)打开食醋的瓶盖,会闻到一股酸味,说明分子具有的性质是
分子是不断运动的
分子是不断运动的
,用pH试纸测定食醋酸度的操作是在玻璃片上放一小片pH试纸,将醋酸溶液滴到试纸上,把显示的颜色与标准色卡比较
在玻璃片上放一小片pH试纸,将醋酸溶液滴到试纸上,把显示的颜色与标准色卡比较
.(4)车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.乙醇与汽油均属于
有机物
有机物
(填“无机物”或“有机物”);乙醇分子中碳元素与氢元素的质量比为4:1
4:1
;若100t汽油中添加11.1
11.1
t乙醇可配制得到含乙醇质量分数为10%的车用乙醇汽油(精确到0.1).(2008?昌平区一模)金属是一类重要的材料,人类生活和生产都离不开金属.
(1)金属在生活中的许多应用都是由金属的物理性质决定的.下表是一些金属的物理性质.
根据表中提供的信息和你的生活经验,解释银的导电性比铜好,为什么导线一般用铜而不用银的原因
(2)如下图是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

①铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼 C.铝的硬度小 D.铝的冶炼相对难
②目前铝合金在多个领域替代易生锈的钢铁,其主要原因是
③现提供药品铁丝、铜丝、银丝、硫酸铜溶液、硫酸亚铁溶液、硝酸银溶液、稀盐酸等,请你设计最佳实验方案确定Fe、Cu、Ag三种金属的活动性顺序.
你选择的药品是:
填写实验报告:
查看习题详情和答案>>
(1)金属在生活中的许多应用都是由金属的物理性质决定的.下表是一些金属的物理性质.
| 物理性质 | 物理性质比较 |
| 导电性(以银的导电性为100作标准) | 银 铜 金 铝 锌 铁 铅 (优) 100 99 74 61 27 17 8 (良) |
| 密度 单位:g/cm3 |
金 铅 银 铜 铁 锌 铝 (大) 19.3 11.3 10.5 8.92 7.86 7.14 2.70 (小) |
| 熔点 单位:℃ |
钨 铁 铜 金 银 铝 锡 (高) 3410 1535 1083 1064 962 660 232 (低) |
| 硬度(以金刚石的硬度为10作标准) | 铬 铁 银 铜 金 铝 铅 (大)9 4-5 2.5-4 2.5-3 2.5-3 2-2.9 1.5(小) |
银虽然导电性强,但是价格昂贵,所以使用铜导线
银虽然导电性强,但是价格昂贵,所以使用铜导线
.请分析灯泡里的灯丝用钨制而不用锡制的原因因为钨的熔点高,用于灯泡里的灯丝使用寿命长
因为钨的熔点高,用于灯泡里的灯丝使用寿命长
.(2)如下图是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

①铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
BD
BD
.A.铝在地壳中含量高 B.铝相对活泼 C.铝的硬度小 D.铝的冶炼相对难
②目前铝合金在多个领域替代易生锈的钢铁,其主要原因是
铝的表面生成一层致密的氧化膜,对铝起到保护作用
铝的表面生成一层致密的氧化膜,对铝起到保护作用
.③现提供药品铁丝、铜丝、银丝、硫酸铜溶液、硫酸亚铁溶液、硝酸银溶液、稀盐酸等,请你设计最佳实验方案确定Fe、Cu、Ag三种金属的活动性顺序.
你选择的药品是:
铁丝、银丝、硫酸铜溶液或铜丝、硫酸亚铁溶液和硝酸银溶液
铁丝、银丝、硫酸铜溶液或铜丝、硫酸亚铁溶液和硝酸银溶液
.填写实验报告:
| 实验步骤 | 实验现象 | 结论及化学方程式 |
某研究性学习小组的同学在一次探究活动中,对一份纯碱样品(含有少量氯化钠)的纯度进行测定,请你参与并回答有关问题.
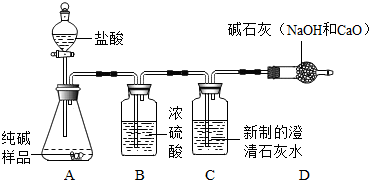
(1)甲同学进行如下操作:
①组装好如图仪器,并检查
②称取6.0g试样放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量盛有新制澄清石灰水的装置C的质量;④打开分液漏斗旋塞滴入盐酸,直到不再产生气泡为止;⑤再次称量装置C 的总质量;⑥计算出样品中碳酸钠的质量分数.
(2)上图B装置的作用是
【意外发现】C瓶中石灰水没有变浑浊,同学们感到惊奇并产生了探究的欲望.
【提出猜想】原因猜想:①是生成的气体中混有盐酸挥发出来的HCl;②是生成的气体流速太快,与石灰水反应产生了可溶性物质[经查资料分析可溶性物质是Ca(HCO3)2,它能与酸反应生成CO2等物质].
【实验探究】甲同学取少量实验后C瓶溶液于试管中,向其中依次滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生.据此判断只有猜想
【交流讨论】对于如何改进实验,乙同学认为:应将盐酸换成稀硫酸,新制的澄清石灰水换成足量NaOH溶液;丙同学认为:应在装置A和B中间插入一个盛有饱和NaHCO3溶液的洗气装置以吸收HCl(CO2不溶于饱和NaHCO3溶液,也不与其反应),并将新制的澄清石灰水换成足量NaOH溶液.
大家讨论后认为:乙同学的方案可行而丙同学的方案不可行.
【请你评价】丙同学方案不可行的原因是
【教师点拨】即便换成稀硫酸和NaOH溶液,反应前后装置中存在的CO2也会使测定出的样品纯度不准确.
【请你改进】在上述基础上,你的措施是
同学们仍称取6.0g试样,用改进完善后的方案重新实验.
【数据处理】装置C实验前后两次称量的质量差为2.2g,则样品的纯度为
【实验反思】若不用上述方法,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是
查看习题详情和答案>>

(1)甲同学进行如下操作:
①组装好如图仪器,并检查
装置的气密性
装置的气密性
;②称取6.0g试样放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量盛有新制澄清石灰水的装置C的质量;④打开分液漏斗旋塞滴入盐酸,直到不再产生气泡为止;⑤再次称量装置C 的总质量;⑥计算出样品中碳酸钠的质量分数.
(2)上图B装置的作用是
干燥CO2气体
干燥CO2气体
; D装置的作用是吸收空气中的CO2和H2O(水蒸气),防止它们进入C装置中,出现误差
吸收空气中的CO2和H2O(水蒸气),防止它们进入C装置中,出现误差
.【意外发现】C瓶中石灰水没有变浑浊,同学们感到惊奇并产生了探究的欲望.
【提出猜想】原因猜想:①是生成的气体中混有盐酸挥发出来的HCl;②是生成的气体流速太快,与石灰水反应产生了可溶性物质[经查资料分析可溶性物质是Ca(HCO3)2,它能与酸反应生成CO2等物质].
【实验探究】甲同学取少量实验后C瓶溶液于试管中,向其中依次滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生.据此判断只有猜想
①
①
(填“①”或“②”)成立.【交流讨论】对于如何改进实验,乙同学认为:应将盐酸换成稀硫酸,新制的澄清石灰水换成足量NaOH溶液;丙同学认为:应在装置A和B中间插入一个盛有饱和NaHCO3溶液的洗气装置以吸收HCl(CO2不溶于饱和NaHCO3溶液,也不与其反应),并将新制的澄清石灰水换成足量NaOH溶液.
大家讨论后认为:乙同学的方案可行而丙同学的方案不可行.
【请你评价】丙同学方案不可行的原因是
NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差
NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差
.【教师点拨】即便换成稀硫酸和NaOH溶液,反应前后装置中存在的CO2也会使测定出的样品纯度不准确.
【请你改进】在上述基础上,你的措施是
两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭
两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭
.同学们仍称取6.0g试样,用改进完善后的方案重新实验.
【数据处理】装置C实验前后两次称量的质量差为2.2g,则样品的纯度为
88.3%
88.3%
.(列出计算过程)【实验反思】若不用上述方法,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是
BaCl2或CaCl2溶液
BaCl2或CaCl2溶液
.