网址:http://m.1010jiajiao.com/timu_id_572130[举报]
太阳是银河系中极为普通的一颗恒星,剧烈的热核反应使之不断地向外辐射能量。太阳辐射的能量绝大部分集中在紫外波段,可见光波段和红外光波段,它们的能量分别占总辐射量的9%、44%和47%。地球的大气层中,基本不变的成分为氧、氮、氩等,占大气总量的99.96%,可变气体成分主要有CO2、水汽和臭氧等,这些气体的含量极小,但对大气物理状况的影响极大。大气臭氧层一般是指高度在离地面10~15Km的大气层,其中臭氧的浓度很低,将它折合成标准状况,其总累积厚度也不过0.3cm,其含量虽小,但对地球的气候和生物影响很大。
(1)大气压强P随距地面高度Z(m)的增大而减小,经验公式为PZ=![]() ,其中P0为地表的气压值,e=2.718。若臭氧层集中在24km的高空处,设在该高度处的温度为—50℃。试估算臭氧层的厚度。
,其中P0为地表的气压值,e=2.718。若臭氧层集中在24km的高空处,设在该高度处的温度为—50℃。试估算臭氧层的厚度。
(2)简要说明臭氧层对地球生物圈的意义。
![]() (3)臭氧层的生消可以简化成如下的反应方程:高层大气中的一个重要的光化学反应是氧分子吸收太阳辐射中波长λ<0.24μm的光子,离解为氧原子,即O2+hν(λ<0.24μm) O+O,由此可形成一系列的反应,其中最重要的是氧原子和氧分子在第三体(M)的参与下形成臭氧,其反应方程式为 。这里的M主要是氧分子或氮分子,它们是在反应过程中同时满足能量守恒和动量守恒所必须的。臭氧在λ<0.18μm的辐射作用下,能离解成氧分子和氧原子,其反应方程式为 。
(3)臭氧层的生消可以简化成如下的反应方程:高层大气中的一个重要的光化学反应是氧分子吸收太阳辐射中波长λ<0.24μm的光子,离解为氧原子,即O2+hν(λ<0.24μm) O+O,由此可形成一系列的反应,其中最重要的是氧原子和氧分子在第三体(M)的参与下形成臭氧,其反应方程式为 。这里的M主要是氧分子或氮分子,它们是在反应过程中同时满足能量守恒和动量守恒所必须的。臭氧在λ<0.18μm的辐射作用下,能离解成氧分子和氧原子,其反应方程式为 。
(4)人类的活动所产生的一些气体,能对大气中的臭氧起到破坏作用。使其含量减少,将造成严重后果,直接威胁到人类的生活和生存。近些年来,屡有在南极或北极,甚至在西藏出现臭氧空洞的报道,引起人们极大的关注。简要说明人类活动产生的那些气体对大气臭氧层能起破坏作用。
查看习题详情和答案>>A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4。请回答:
(1)若Y是黄绿色气体,则该反应的离子方程式是 _____________________________;将Y与等物的量的SO2充分混合后通入品红溶液,未见其褪色,原因是__________________________________________(请用化学方程式解释说明)。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶
液为某浓酸,则反应所得的氧化产物的化学式为 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,而且A可溶于X溶液中:
① A元素的元素符号为 ,则A与B的反应中氧化剂与还原剂的物质的量之比是 。
② 若含a mol X的溶液溶解了一定量A后,此时溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量为 mol(用含a代数式表示);为保证A与B充分反应后最终所得的溶液中同时含有上述两种金属阳离子,则此时B与A的质量比应满足的取值范围是 。
查看习题详情和答案>>
又已知:每消耗1mol H2O2则生成2mol H2O和1mol O2.
请回答下列问题:
(1)请配平.
(2)指出:反应中的氧化剂是
(3)我国的科学家经过科学探索,发现将经干燥空气稀释的氯气通入填充有固体亚氯酸钠(NaClO2)的反应柱内可制得ClO2和NaCl.请写出反应方程式:
(4)若生成8.96L O2(标准状况),则转移的电子的量为
(1)某工厂采用氨-硫酸铵治理含硫烟气和同时吸收焦炉气中的氨,其工艺流程图如图1:

①从环境保护的角度看,采用上述工艺可防止
②氨气吸收塔中发生反应的离子方程式为
(2)有学者提出利用Fe3+的氧化性,将SO2氧化成SO42-而实现SO2的回收利用.
①图2实验Ⅰ可采用图3装置模拟测定烟气中SO2的体积分数.X溶液可以选用
②图2实验Ⅰ还可采用下列方案测定SO2的体积分数,取280mL(标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.020mol/L的K2Cr2O7溶液滴定反应生成的Fe2+,至终点消耗K2Cr2O7溶液25.00mL.尾气中SO2的体积分数为
已知:Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)
③假设实验Ⅱ在标准状况下进行,且已知混合气体流量.为测定转化器中SO2氧化成SO42-的转化率,该实验中还需测定的数据有
实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体.
(1)该小组作出此推测的理由是:
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2mol/L的H2C2O4标准溶液、0.1mol/L的酸性KMnO4标准溶液、酸碱指示剂.
b.实验装置设计及组装(加热及夹持装置均已略去)
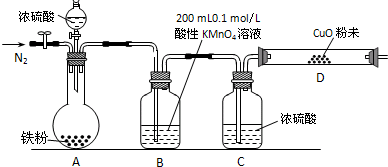
【实验过程及数据处理】
(2)B中发生反应的离子方程式为:
(3)实验前先通入一段时间的N2,其目的是
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25mL,用H2C2O4标准溶液进行滴定.
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平.
②滴定达到终点时的现象是
③重复滴定两次,平均每次耗用H2C2O4标准溶液15.63mL,则铁与浓硫酸反应产生的SO2气体
的物质的量为