摘要:2.1问卷调查.为了确定课题研究方向和可行性.课题组对永顺县高中化学实验教学从实验设备.实验员数和化学老师这三方面进行了问卷调查.调查结果表明高中化学课堂实验教学是不够理想的.主要体现在两大方面:①县各学校实验教学条件差.②教师自身新教材实验教学认识不够.重视不够.详细情况见 .
网址:http://m.1010jiajiao.com/timu_id_4437122[举报]
 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),
设计实验方案来研究影响反应速率的因素.
(1)甲同学研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. |
反应快慢:Mg>Fe>Cu | 反应物的性质越活泼,反应速度越快 |
反应物本身的性质
反应物本身的性质
对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持温度
温度
相同.(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验.完成该实验应选用的实验药品是
0.5mol/L、2mol/L
0.5mol/L、2mol/L
;应该测定的实验数据是测定一定时间产生气体的体积或测定产生一定体积的气体所需时间
测定一定时间产生气体的体积或测定产生一定体积的气体所需时间
.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:
(2)某工程师为了从使用过的腐蚀废液(不含FeCl3)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述试验过程中②⑤的化学式:②
请写出①⑥两步反应的离子方程式:
查看习题详情和答案>>
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:
2FeCl3+Cu═2FeCl2+CuCl2
2FeCl3+Cu═2FeCl2+CuCl2
;若反应过程中有2mol电子发生转移,会有64
64
g Cu溶解.(2)某工程师为了从使用过的腐蚀废液(不含FeCl3)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述试验过程中②⑤的化学式:②
FeCl2
FeCl2
,⑤FeCl2
FeCl2
.请写出①⑥两步反应的离子方程式:
Fe+Cu2+═Cu+Fe2+
Fe+Cu2+═Cu+Fe2+
;2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
.在阅读资料时,小红发现,儿童从空气中吸入的铅量是成人吸入量的1.6~1.7倍.为了探讨这个现象,她展开了如下的研究.利用所学知识完成以下填空.
(1)课题名称为:
(2)通过取样分析,得到了下表实验数据:
分析以上实验数据,可以得出的结果是
废水样品
含Pb2+溶液
沉淀
(3)步骤中过滤需要的玻璃仪器是
(4)步骤中a操作称为
(5)通过研究,小红提出了一系列降低铅对环境污染的建议,下列建议中不恰当的事
A.使用无铅汽油 B.开发新的无铅燃料
C.倡导使用铅蓄电池作动力的电动车 D.燃煤电厂、金属冶炼厂的废气经除尘后排放.
查看习题详情和答案>>
(1)课题名称为:
近地面不同高度空气含铅量的研究:
近地面不同高度空气含铅量的研究:
(2)通过取样分析,得到了下表实验数据:
| 离地面高度(m) | 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 2.0 |
| 空气中铅的浓度(μg/m3) | 1.10 | 0.98 | 0.91 | 0.72 | 0.66 | 0.54 | 0.50 |
离地面越低(高),含铅量越高(低)
离地面越低(高),含铅量越高(低)
造成此结果的原因可能是铅和铅化合物密度大
铅和铅化合物密度大
在走访调查中,小红观察到某乡镇颜料厂排出的废水带有颜色,经鉴定含有铅.为了测定废水中铅的浓度,他设计了如下实验步骤:废水样品
| 化学处理 |
| K2CrO4 |
| 过滤 |
| 洗涤 |
| a |
| 称量 |
(3)步骤中过滤需要的玻璃仪器是
烧杯
烧杯
、漏斗
漏斗
和玻璃棒.(4)步骤中a操作称为
烘干
烘干
,缺少此操作,测得结果偏高
偏高
(填“偏高”、“偏低”、或“无影响”).(5)通过研究,小红提出了一系列降低铅对环境污染的建议,下列建议中不恰当的事
C
C
A.使用无铅汽油 B.开发新的无铅燃料
C.倡导使用铅蓄电池作动力的电动车 D.燃煤电厂、金属冶炼厂的废气经除尘后排放.
 环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.
环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.(1)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,反应方程式可表示为:CO+Hb?O2
 O2+Hb?CO
O2+Hb?CO实验表明,c(Hb?CO)即使只有c(Hb?O2)的 1/50,也可造成人的智力损伤.
已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol?L-1,若使c(Hb?CO)小于c(Hb?O2)的 1/50,则吸入肺部CO的浓度不能超过
1.0×10-6
1.0×10-6
mol?L-1.(2)汽车尾气治理的方法之一是在汽车的排气管上安装一个“催化转化器”.
已知反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)△H=-113kJ?mol-1
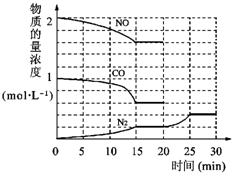
N2(g)+2CO2(g)△H=-113kJ?mol-1①为了模拟催化转化器的工作原理,在t℃时,将2molNO与1mol CO充入lL反应容器中,反应过程中NO(g)、CO(g)、N2(g)物质的量浓度变化如右下图所示.反应进行到15min时,NO的平均反应速率为
| 0.4 |
| 15 |
| 0.4 |
| 15 |
②观察在20min~30min内N2(g)发生变化的曲线图,判断引起该变化的条件可能是
b
b
;a.加入催化剂
b.降低体系温度
c.缩小容器体积为0.5L
d.增加CO2的物质的量
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①上述正向反应是:
放热
放热
反应(填“放热”、“吸热”).②某温度下上述反应平衡时,恒容、升高温度,正反应速率
增大
增大
(填“增大”、“减小”或“不变”),容器内混合气体的压强增大
增大
(填“增大”、“减小”或“不变”).③在830℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有
B、C
B、C
(选填A、B、C、D).| A | B | C | D | |
| n(CO2) | 3 | 1 | 0 | 1 |
| n(H2) | 2 | 1 | 0 | 1 |
| n(CO) | 1 | 2 | 3 | 0.5 |
| n(H2O) | 5 | 2 | 3 | 2 |
为了探究浓度对硫酸氧化性的影响,某学习小组进行了以下探究活动:
[探究一]称取无锈铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
(1)甲同学认为X中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,请选择下列试剂,设计简单的实验方案(简述操作过程、现象和结论)
供选用试剂:a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
(2)乙同学为了测定气体Y中SO2的含量,设计如下三种方案:
方案Ⅰ.取672mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g.
方案Ⅱ.向VmL c mol?L-1酸性高猛酸钾溶液中缓慢通入Y气体aL(标准状况),溶液恰好完全褪色.
方案Ⅲ,取VL(标准状况)气体Y缓慢通入足量的氢氧化钡溶液中,充分反应后,过滤、洗涤、烘干,称得固体质量为mg.
①其中不合理的方案是
②选择合理方案的数据计算气体Y中SO2的体积分数(用含未知数的代数式表示)
[探究二]分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体.为此设计了下列探究实验装置(图中夹持装置已省略).
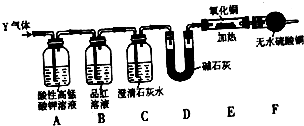
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有CO2的实验现象:
(5)有同学根据“F干燥管无水硫酸铜是否变蓝色”确认Y气体中是否有氢气,你认为是否可靠?
查看习题详情和答案>>
[探究一]称取无锈铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
(1)甲同学认为X中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,请选择下列试剂,设计简单的实验方案(简述操作过程、现象和结论)
取少量X溶液装于试管,向试管中滴加酸性高猛酸钾溶液,若溶液褪色,则证明X溶液中含有Fe2+,否则不含Fe2+
取少量X溶液装于试管,向试管中滴加酸性高猛酸钾溶液,若溶液褪色,则证明X溶液中含有Fe2+,否则不含Fe2+
.供选用试剂:a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
(2)乙同学为了测定气体Y中SO2的含量,设计如下三种方案:
方案Ⅰ.取672mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g.
方案Ⅱ.向VmL c mol?L-1酸性高猛酸钾溶液中缓慢通入Y气体aL(标准状况),溶液恰好完全褪色.
方案Ⅲ,取VL(标准状况)气体Y缓慢通入足量的氢氧化钡溶液中,充分反应后,过滤、洗涤、烘干,称得固体质量为mg.
①其中不合理的方案是
方案III
方案III
,理由是生成BaCO3和BaSO4两种沉淀,无法计算SO2的体积
生成BaCO3和BaSO4两种沉淀,无法计算SO2的体积
.②选择合理方案的数据计算气体Y中SO2的体积分数(用含未知数的代数式表示)
66.7%或
×100%
| 7cV |
| 125a |
66.7%或
×100%
.| 7cV |
| 125a |
[探究二]分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体.为此设计了下列探究实验装置(图中夹持装置已省略).

(3)装置A中试剂的作用是
吸收并除去SO2
吸收并除去SO2
.(4)简述确认气体Y中含有CO2的实验现象:
B中品红溶液不褪色,C中澄清石灰水变浑浊
B中品红溶液不褪色,C中澄清石灰水变浑浊
.(5)有同学根据“F干燥管无水硫酸铜是否变蓝色”确认Y气体中是否有氢气,你认为是否可靠?
不可靠
不可靠
(填“可靠”或“不可靠”),简述理由:空气中的水蒸气进入F装置,也可使无水硫酸铜变蓝色
空气中的水蒸气进入F装置,也可使无水硫酸铜变蓝色
.