摘要:二氧化硫的性质 (1)物理性质:无色.有刺激性气味的有毒气体.易溶于水. (2)化学性质 ①酸性氧化物的通性. ②与水反应 SO2+H2O H2SO3 ③氧化性 SO2+H2S===3S↓+2H2O ④还原性 2SO2+O2 2SO3 ⑤能使品红溶液褪色(该性质用来检验SO2). <说明>:不要求学生掌握所有转化反应的化学方程式.
网址:http://m.1010jiajiao.com/timu_id_4435106[举报]
二氧化硫是污染大气形成酸雨的主要有害物质之一,如果了解二氧化硫的性质,它在我们的生活中也有广泛的用途.
(1)下列可产生二氧化硫污染大气的是 .(填序号).
A.含硫矿石的冶炼 B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放 D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份雨水样品,每隔一段时间测定该雨水样品的pH变化数据如下
分析雨水样品pH变化的原因(用文字和化学方程式说明) .
(3)某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告.
(4)目前通常采用滴定法测定食品中残留二氧化硫的含量.具体实验方法主要是:样品经处理后,加入氢氧化钾使残留的二氧化硫以亚硫酸盐的形式固定,再加入硫酸使二氧化硫游离,用碘标准溶液滴定二氧化硫.在滴定时用 (填名称)作指示剂,滴定终点的现象是 .
查看习题详情和答案>>
(1)下列可产生二氧化硫污染大气的是
A.含硫矿石的冶炼 B.大量化石燃料的燃烧
C.大量烟花爆竹的燃放 D.硫酸厂排放的工业尾气
(2)某课外小组采集了一份雨水样品,每隔一段时间测定该雨水样品的pH变化数据如下
| 测试时间段 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(3)某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告.
| 序号 | 二氧化硫的性质 | 主要操作和现象 | 化学方程式 |
| ① | 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 | ||
| ② | 氧化性 | ||
| ③ | 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色变为无色 |
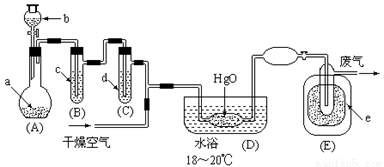
氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,仅铁架台和夹持仪器已略去。
部分物质的有关物理数据如下:
|
化学式 |
熔点(单位:℃) |
沸点(单位:℃) |
|
N2 |
-209.86 |
-195.8 |
|
O2 |
-218.4 |
-183 |
|
CO2 |
-57 |
/ |
|
NH3 |
-77.3 |
-33.35 |
|
Cl2 |
-101 |
-34.6 |
试回答:
(1)A中深色固体与无色液体制备气体的离子方程式: 。
(2)B中盛有液体c是饱和 ,C中的液体d是浓硫酸。?
(3)氧化二氯制备出之后,要冷却为固态才便于操作和贮存,则E中的保温瓶中盛有致冷剂,它应是
(在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是反应物中过量的 。
(4)装置D、E间的连接方式与A、B、C间的连接方式有明显的区别,这区别是D、E中无 管、塞,用这些不同的连接方式的主要理由是氧化二氯接触有机物而 。
查看习题详情和答案>>
氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,仅铁架台和夹持仪器已略去。
部分物质的有关物理数据如下:
| 化学式 | 熔点(单位:℃) | 沸点(单位:℃) |
| N2 | -209.86 | -195.8 |
| O2 | -218.4 | -183 |
| CO2 | -57 | / |
| NH3 | -77.3 | -33.35 |
| Cl2 | -101 | -34.6 |
试回答:
(1)A中深色固体与无色液体制备气体的离子方程式: 。
(2)B中盛有液体c是饱和 ,C中的液体d是浓硫酸。?
(3)氧化二氯制备出之后,要冷却为固态才便于操作和贮存,则E中的保温瓶中盛有致冷剂,它应是
(在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是反应物中过量的 。
(4)装置D、E间的连接方式与A、B、C间的连接方式有明显的区别,这区别是D、E中无 管、塞,用这些不同的连接方式的主要理由是氧化二氯接触有机物而 。 查看习题详情和答案>>
 铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.(1)铁元素在元素周期表中的位置是
第四周期第VIII族
第四周期第VIII族
.(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为
4Al+3O2+6H2O=4Al(OH)3
4Al+3O2+6H2O=4Al(OH)3
;②电池中NaCl的作用是
增强溶液的导电能力
增强溶液的导电能力
.(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
,此时向溶液中加入8g CuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为1.12
1.12
L.(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式
Al2O3+3C+3Cl2
2AlCl3+3CO.
| ||
Al2O3+3C+3Cl2
2AlCl3+3CO.
.
| ||
(5)三氧化二铁和氧化亚铜(Cu2O)都是红色粉末,常用作颜料.已知氧化亚铜溶于稀硫酸生成Cu和CuSO4.取少量Fe2O3和Cu2O组成的混合物放入足量稀硫酸中.
①此过程中发生的反应有(用离子方程式表示):
Fe2O3+6H+=2Fe3++3H2O;
Cu2O+2H+=Cu+Cu2++H2O
Cu2O+2H+=Cu+Cu2++H2O
;Cu+2Fe3+=2Fe2++Cu2+
Cu+2Fe3+=2Fe2++Cu2+
②设计实验证明反应后所得溶液中铁元素可能存在形式
取少量所得溶液于试管中,向其中滴加硫氰化钾溶液,若溶液变红则说明存在铁离子,反之则无,另取少量所得溶液于试管中,向其中滴加酸性高锰酸钾溶液,溶液褪色说明含有亚铁离子,不褪色说明没有亚铁离子
取少量所得溶液于试管中,向其中滴加硫氰化钾溶液,若溶液变红则说明存在铁离子,反之则无,另取少量所得溶液于试管中,向其中滴加酸性高锰酸钾溶液,溶液褪色说明含有亚铁离子,不褪色说明没有亚铁离子
.③若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu2O)
>
>
n(Fe2O3).(填“>”、“<”或“=”)(2013?闵行区一模)氯化硫酰(SO2Cl2)主要用作氯化剂.它是一种无色液体,熔点-54.1℃,沸点69.1℃.氯化硫酰可用干燥的二氧化硫和氯气在活性炭催化剂存在下反应制取:SO2(g)+Cl2(g)
SO2Cl2(l)+97.3kJ
(1)试写出常温常压下化学平衡常数K的表达式:K=
;
若在此条件下,将化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是
a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(2)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是
a.缩小容器体积 b.使用催化剂 c.增加SO2浓度 d.升高温度
(3)在100℃时,往上述平衡体系中加入37Cl2,一段时间后,则平衡体系中含有37Cl的物质有
a.只有37Cl2 b.只有SO237Cl2 c.37Cl2和SO237Cl2 d.无法判断
(4)下列描述中能说明上述反应已达平衡的是
a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(5)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是
查看习题详情和答案>>
| 活性炭 |
(1)试写出常温常压下化学平衡常数K的表达式:K=
| 1 |
| c(SO2)?c(Cl2) |
| 1 |
| c(SO2)?c(Cl2) |
若在此条件下,将化学平衡常数K增大,化学反应速率v正也增大,可采取的措施是
d
d
(选填编号).a.降低温度 b.移走SO2Cl2
c.增加反应物浓度 d.无法满足上述条件
(2)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是
ac
ac
(选填编号).a.缩小容器体积 b.使用催化剂 c.增加SO2浓度 d.升高温度
(3)在100℃时,往上述平衡体系中加入37Cl2,一段时间后,则平衡体系中含有37Cl的物质有
c
c
(选填编号).a.只有37Cl2 b.只有SO237Cl2 c.37Cl2和SO237Cl2 d.无法判断
(4)下列描述中能说明上述反应已达平衡的是
bd
bd
(选填编号).a.υ(Cl2)=υ(SO2) b.容器中气体压强不随时间而变化
c.c(Cl2):c(SO2)=1:1 d.容器中气体颜色不随时间两变化
(5)300℃时,体积为1L的密闭容器中充入16.20g SO2Cl2,达到平衡时容器中含SO2 7.616g.若在上述中的平衡体系中,再加入16.20g SO2Cl2,当再次达平衡时,容器中含SO2的质量范围是
7.616g<m(SO2)<15.232g
7.616g<m(SO2)<15.232g
.