网址:http://m.1010jiajiao.com/timu_id_4435054[举报]
(1)氮肥厂的氨氮废水经过初步处理后可得到低浓度氨氮废水,后续处理流程如下:

过程II:加入甲醇,NO3-和甲醇反应转化CO2和N2。
请写出过程I步的离子方程式:_________________ 。
(2)Hg是水体污染的重金属元素之一。水溶液中二价汞的主要存在形态与Cl-、OH-的浓度关系如图所示[图中的物质或粒子只有Hg(OH)2为难溶物; pCl=-1gc(Cl-)]

A.为了防止Hg2+水解,配制Hg(NO3)2溶液时应将Hg(NO3)2固体溶于浓硝酸后再稀释。 B.当c(Cl-) =10-1 mol·L-1时,汞元素一定全部以HgCl42-形式存在
C.HgCl2是一种弱电解质,其电离方程式是:HgCl2=HgCl+ + Cl-
D.当溶液pH保持在4,pCl由2改变至6时,可使HgCl2转化为Hg(OH)2
②HgCl2又称“升汞”,熔点549K,加热能升华,其晶体是_________(填晶体类型)。
(3)汽车尾气是城市空气污染的一个重要因素,常用以下反应净化汽车尾气:
2NO(g)+2CO(g)
 2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表:
2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表: 
③在上述条件下该反应能够自发进行,如果把温度从T1℃升高到T2℃,平衡常数K将__________(填写“变大”、“变小”、“不变”)。
④一种CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似燃料电池,其中的固体电解质是Y2O3-Na2O,O2ˉ可以在其中自由移动,负极的反应式为____________。
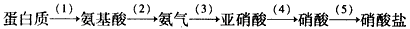
(3)请你从控制污染源的角度,提出两条防止“水华”现象的措施:
①_______________________;②________________________。
氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力。下图是自然界中氮的循环图,请回答有关问题。

(1)从空气中获取氮是人类长久以来追求的目标。下列有关说法正确的是_________(填序号)。
a.图中①②③④⑤都属于自然界的固氮过程
b.在过程⑥中,氮元素的化合价降低
c.反应②的化学方程式是N2 +O2
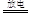 2NO
2NO
d.德国化学家哈伯发明了合成氨工艺,其主要反应如下2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)氨经氧化后可得到硝酸,而硝酸能与氨形成含氮量很高的肥料NH4NO3,施用于土壤而实现非自然形式的氮循环。但这种肥料不适宜与碱性物质共用,否则会降低肥效,其原因是_________________________________(用离子方程式表示)。
(3)人类活动对氮循环产生着明显的影响。汽车尾气中的NO,是造成光化学烟雾的物质之一,但NO对人体又起着独特的生理作用,被誉为“明星分子”,有三位科学家因此项研究成果而获得1998年诺贝尔奖。上述事实说明我们应辨证地看待化学物质的作用。科技人员已经找到了一些解决NO排放的方法。在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为空气中的两种成分。气体在催化剂表面吸附与解吸作用的机理如下图所示。
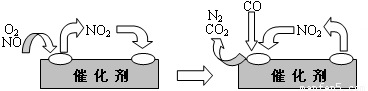
写出上述变化中的总化学反应方程式____________________________________。
查看习题详情和答案>>
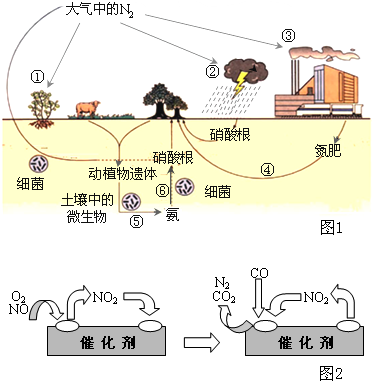 氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力.如图1是自然界中氮的循环图,请回答有关问题.
氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力.如图1是自然界中氮的循环图,请回答有关问题.(1)从空气中获取氮是人类长久以来追求的目标.下列有关说法正确的是
a.图中①②③④⑤都属于自然界的固氮过程
b.在过程⑥中,氮元素的化合价降低
c.反应②的化学方程式是N2+O2
| ||
d.德国化学家哈伯发明了合成氨工艺,其主要反应如下
2NH4Cl+Ca(OH)2
| ||
(2)氨经氧化后可得到硝酸,而硝酸能与氨形成含氮量很高的肥料NH4NO3,施用于土壤而实现非自然形式的氮循环.但这种肥料不适宜与碱性物质共用,否则会降低肥效,其原因是
(3)人类活动对氮循环产生着明显的影响.汽车尾气中的NO,是造成光化学烟雾的物质之一,但NO对人体又起着独特的生理作用,被誉为“明星分子”,有三位科学家因此项研究成果而获得1998年诺贝尔奖.上述事实说明我们应辨证地看待化学物质的作用.
科技人员已经找到了一些解决NO排放的方法.在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为空气中的两种成分.气体在催化剂表面吸附与解吸作用的机理如图2所示.
写出上述变化中的总化学反应方程式
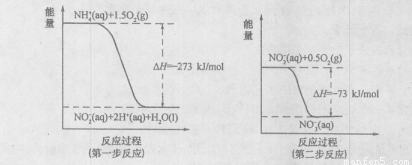
(I)某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下:
 [来源:学,科,网]
[来源:学,科,网]
(1)1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
(Ⅱ)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO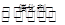 2CO2+N2
△H
2CO2+N2
△H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
C(NO)(×10-4mol·L-1) |
10.0 |
4.50 |
2.50 |
1.50 |
1.00 |
1.00 |
|
C(CO)(×10-3mol·L-1) |
3.60 |
3.05 |
2.85 |
2.75 |
2.70 |
2.70 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”)
(2)前2s内的平均反应速率v(N2)= ;
(3)在该温度下,反应的平衡常数K= (只写出计算结果);
(4)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,部分实验条件如下表:
|
实验编号 |
T/℃ |
NO初始浓度/mol·L-1 |
CO初始浓度/mol·L-1 |
催化剂的比表面积/m2·g-1 |
|
I |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
|
II |
280 |
1.20×10-3 |
5.80×10-3 |
124 |
|
III |
350 |
1.20×10-3[来源:学.科.网] |
5.80×10-3 |
124 |
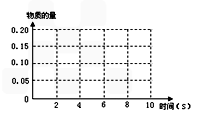
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
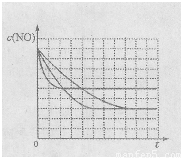
(5)有人认为:催化剂比表面积增大,会提高NO和CO的反应效率,从而使污染物NO和CO的转化率提高。请用化学基本理论对此观点进行评价: 。
查看习题详情和答案>>