摘要:实验探究.自主归纳.
网址:http://m.1010jiajiao.com/timu_id_4435006[举报]
某实验小组开展自主实验活动,学校实验室提供如下实验试剂和实验装置:实验试剂:A.浓盐酸 B.稀盐酸 C.浓硫酸 D.稀硫酸 E.MnO2粉末F.Na2SO3晶体 G.Na2SO3稀溶液 H.NaOH稀溶液 I.品红溶液
实验装置如图1:
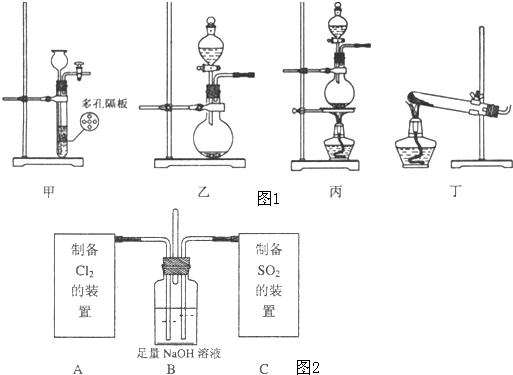
I.该小组拟制备Cl2和SO2两种气体,请为其选择适当的试剂和装置(用字母表示)并填入下表:
上述制备Cl2的反应的离子方程式是:
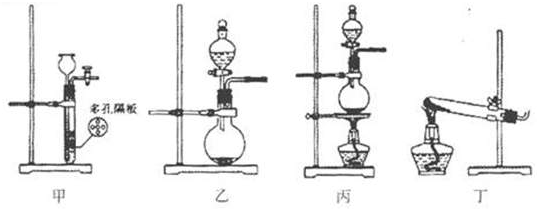
II.该小组进一步探究Cl2和SO2两种气体的化学性质,设计如图2装置.
首先将C中少量SO2通入B中,请书写SO2与过量NaOH稀溶液反应的化学方程式: ;待上述反应完全后再将A中Cl2通入B中充分反应,此时溶液中孝牢本旱夸李的阴离子是: .(不考虑空气中的CO2的影响)
为验证溶液中可能大量存在的阴离子,该小组又设计了若干实验方案,其中验证二价阴离子的实验简要操作及结论是: .
查看习题详情和答案>>
实验装置如图1:

I.该小组拟制备Cl2和SO2两种气体,请为其选择适当的试剂和装置(用字母表示)并填入下表:
| 气体 | 试剂 | 装置 |
| Cl2 | ||
| SO2 |
II.该小组进一步探究Cl2和SO2两种气体的化学性质,设计如图2装置.
首先将C中少量SO2通入B中,请书写SO2与过量NaOH稀溶液反应的化学方程式:
为验证溶液中可能大量存在的阴离子,该小组又设计了若干实验方案,其中验证二价阴离子的实验简要操作及结论是:
某实验小组开展自主实验活动,学校实验室提供如下实验试剂和实验装置:实验试剂:
A.浓盐酸 B.稀盐酸 C.浓硫酸 D.稀硫酸 E.MnO2粉末 F.Na2SO3晶体
G.Na2SO3稀溶液 H.NaOH稀溶液 I.品红溶液
实验装置:
I.该小组拟制备Cl2和SO2两种气体,请为其选择适当的试剂和装置(用字母表示)并填入下表:
上述制备Cl2的反应的离子方程式是: .
II.该小组进一步探究Cl2和SO2两种气体的化学性质,设计如图装置.
首先将C中少量SO2通入B中,请书写SO2与过量NaOH稀溶液反应的化学方程式: ;为验证此时溶液中大量存在的阴离子,该小组又设计了若干实验方案,其实验简要操作及结论是: .
待SO2与过量NaOH稀溶液反应完全后再将过量Cl2通入B中充分反应,此时溶液中一定能大量存在的阴离子是: .(不考虑空气中的CO2的影响)
查看习题详情和答案>>
A.浓盐酸 B.稀盐酸 C.浓硫酸 D.稀硫酸 E.MnO2粉末 F.Na2SO3晶体
G.Na2SO3稀溶液 H.NaOH稀溶液 I.品红溶液
实验装置:

I.该小组拟制备Cl2和SO2两种气体,请为其选择适当的试剂和装置(用字母表示)并填入下表:
| 气体 | 试剂 | 装置 |
| Cl2 | ||
| SO2 |
II.该小组进一步探究Cl2和SO2两种气体的化学性质,设计如图装置.

首先将C中少量SO2通入B中,请书写SO2与过量NaOH稀溶液反应的化学方程式:
待SO2与过量NaOH稀溶液反应完全后再将过量Cl2通入B中充分反应,此时溶液中一定能大量存在的阴离子是:
下面是某同学研究氯气性质过程中的一个片断.请你帮助他完成部分实验并补全实验记录.
【观察】氯气的颜色、状态:
【预测】氯气是一种非金属单质,它可能具有性质有
从元素化合价的角度分析,它可能具有性质有
【实验探究】
【实验结论】(1)通过比较氯气和曾经学习过的氧气等非金属单质的性质,可推知氯气的化学性
(2)在上述过程中,该同学都用到了哪些研究物质性质的方法?
(3)说明闻气体气味的方法.
查看习题详情和答案>>
【观察】氯气的颜色、状态:
黄绿色
黄绿色
色气体
气体
状态;闻氯气的气味:有刺激性
有刺激性
气味.【预测】氯气是一种非金属单质,它可能具有性质有
能与钠、铁、铜等金属发生化合反应,与氢气发生化合反应
能与钠、铁、铜等金属发生化合反应,与氢气发生化合反应
.从元素化合价的角度分析,它可能具有性质有
与具有还原性的物质发生氧化还原反应
与具有还原性的物质发生氧化还原反应
.【实验探究】
| 实验内容 | 实验操作 | 实验现象 | 推断生成物 |
| 氯气与铁反应 | |||
| 氯气与氢气反应 | |||
| 氯气与碘化钾溶液反应 |
比较活泼
比较活泼
,能与铁、铜、钠等金属,氢气、红磷、硫等非金属、KI、FeCl2、Na2SO3等具有还原性的化合物
铁、铜、钠等金属,氢气、红磷、硫等非金属、KI、FeCl2、Na2SO3等具有还原性的化合物
反应.(2)在上述过程中,该同学都用到了哪些研究物质性质的方法?
观察法、实验法、分类法、比较法
观察法、实验法、分类法、比较法
.(3)说明闻气体气味的方法.
用手在集气瓶口轻轻扇动,使少量的气体飘入鼻孔
用手在集气瓶口轻轻扇动,使少量的气体飘入鼻孔
.(2009?宿迁模拟)某校化学研究性学习小组在学习了乙醇、乙醛的性质后,进行了以下实验探究.
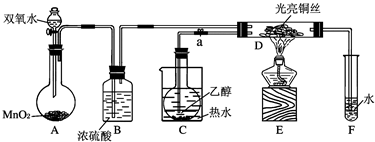
试回答以下问题:
(1)按上图(夹持装置仪器已省略)进行乙醇在铜催化条件下与氧气反应制乙醛的实验,安装好仪器装置,在加入药品前,首先应进行的操作是
(2)实验开始时,先关闭止水夹a,打开分液漏斗活塞,在铜丝部位加热片刻,然后打开止水夹a,在 D处观察到的实验现象为
(3)取反应后F中的少量溶液滴入新制的氢氧化铜碱性悬浊液中并加热至沸腾,观察到有红色沉淀产生.有同学认为红色沉淀的成分可能是Cu2O或Cu或Cu2O与Cu的混合物.
通过查阅资料获知:①在酸性条件下,Cu2O+2H+=Cu2++Cu+H2O;②Cu、CuO在空气中高温灼烧均生成Cu2O.
为了验证红色沉淀的成分他们设计了如下实验:
方案1 取少量该红色沉淀,往其中加入足量的稀硝酸,观察反应现象.
方案2 取少量该红色沉淀,往其中加入足量的稀硫酸,观察反应现象.
方案3 称取经充分干燥的该红色沉淀a g,在空气中高温灼烧,并在干燥器里冷却,再称重,反复多次直至恒重,称得固体的质量为b g,比较a、b的大小关系.
上述三个方案中能够确定该红色沉淀成分的是
其他方案不能确定的原因是
查看习题详情和答案>>

试回答以下问题:
(1)按上图(夹持装置仪器已省略)进行乙醇在铜催化条件下与氧气反应制乙醛的实验,安装好仪器装置,在加入药品前,首先应进行的操作是
检查装置的气密性
检查装置的气密性
.C中热水的作用是产生平稳的乙醇蒸气
产生平稳的乙醇蒸气
.(2)实验开始时,先关闭止水夹a,打开分液漏斗活塞,在铜丝部位加热片刻,然后打开止水夹a,在 D处观察到的实验现象为
变黑的铜丝又变红,出现交替变化
变黑的铜丝又变红,出现交替变化
,D处反应的化学方程式为2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
.| Cu |
| △ |
(3)取反应后F中的少量溶液滴入新制的氢氧化铜碱性悬浊液中并加热至沸腾,观察到有红色沉淀产生.有同学认为红色沉淀的成分可能是Cu2O或Cu或Cu2O与Cu的混合物.
通过查阅资料获知:①在酸性条件下,Cu2O+2H+=Cu2++Cu+H2O;②Cu、CuO在空气中高温灼烧均生成Cu2O.
为了验证红色沉淀的成分他们设计了如下实验:
方案1 取少量该红色沉淀,往其中加入足量的稀硝酸,观察反应现象.
方案2 取少量该红色沉淀,往其中加入足量的稀硫酸,观察反应现象.
方案3 称取经充分干燥的该红色沉淀a g,在空气中高温灼烧,并在干燥器里冷却,再称重,反复多次直至恒重,称得固体的质量为b g,比较a、b的大小关系.
上述三个方案中能够确定该红色沉淀成分的是
方案3
方案3
,其他方案不能确定的原因是
方案1的三种情况现象相同,无法确定;方案2中Cu2O和Cu2O与Cu的混合物在稀硫酸中反应的现象相同,也无法确定
方案1的三种情况现象相同,无法确定;方案2中Cu2O和Cu2O与Cu的混合物在稀硫酸中反应的现象相同,也无法确定
.