网址:http://m.1010jiajiao.com/timu_id_419339[举报]
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。
(1)写出甲同学实验中两个主要的化学方程式 , 。
(2)甲同学设计的实验 (填能或不能)验证乙炔溴与发生加成反应,其理由是
(a)使溴水褪色的反应,未必是加成反应 (b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔 (d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是 ,它与溴水反应的化学方程式是 ;因此在验证过程中必须全部除去。
(4)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是
查看习题详情和答案>>①用pH试纸鉴别浓硫酸与浓硝酸
②用硝酸银溶液区分二氧化氮和溴蒸气
③酒精灯被碰倒洒出酒精着火时,迅速用湿抹布扑盖
④用酸性高锰酸钾溶液除去二氧化碳中混有的少量二氧化硫
⑤温度计被摔坏导致水银散落到地面上,应立即用水冲洗水银
⑥称量NaOH固体时,把NaOH固体放在有滤纸的托盘上称量
⑦为了提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液进行酸化
⑧检验氯代烃中的氯元素时,可先加氢氧化钠溶液并加热,再加入硝酸银溶液来进行检验
(2)实验室中利用电石和水反应制取一定量乙炔来进行其性质实验(通入溴水、酸性KMnO4溶液),最后点燃(如下图)。完成下列问题:

①制取乙炔的化学方程式为:__________________________________________。
②实验前,应检查气体发生装置(如上图虚线框内装置)的气密性。某同学用双手捂住烧瓶,把导气管伸入水面下,但无任何气泡冒出,则出现此现象的原因可能是___________(填代号)。
A.没有关闭分液漏斗的活塞
B.橡皮塞上的孔与导管不匹配或橡皮塞与分液漏斗不匹配
C.导管伸入水面下太深
D.烧瓶容积较大
③实验室用上图方法点燃乙炔,由于乙炔在空气中燃烧会产生浓烈的黑烟,所以在实验时点燃后要迅速熄灭火焰。试用一种简单的、安全的操作方法熄灭火焰:_________________________________。
查看习题详情和答案>>A.《化学与生活》
(1)食品和药品关系人的生存和健康.
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”.食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质.从化学成分看,纤维素是一种
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)蛋白质是生命的基础,没有蛋白质就没有生命.请回答下列问题:
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和
②人体摄入的蛋白质在胃蛋白酶和胰蛋白酶的作用下,水解成
③维生素C是一种重要维生素,能防治坏血病.用淀粉溶液、碘水为试剂,验证维生素C具有还原性的实验操作和现象是
(3)材料是人类赖以生存和发展的重要物质基础.
①普通玻璃是生活中常用的硅酸盐材料,其主要成分是Na2SiO3、CaSiO3和
| ||
| ||
②通常使用的钢铁是铁和
③天然橡胶(生胶)是线型高分子,因高分子链上有双键易老化,工业上常将它与含硫物质作用转变成为体型的网状分子的
B.《有机化学》
(1)有机物含有的官能团不同,性质也有差异.
①1mol下列有机物可与2mol溴单质发生加成反应的是
A.乙烯 B.乙炔 C.乙烷
②下列有机物中,核磁共振氢谱只有一个吸收峰的是
A.苯 B.苯酚 C.苯甲酸
③下列有机物中,能发生银镜反应的是
A.乙酸乙酯 B.乙醇 C.葡萄糖
(2)分子式为C4H10O,属于醇的同分异构体有




(3)科学家常采用将药物连接在高分子载体上,制成缓释长效药物.已知某种解热镇痛类药物,其结构简式如图甲,把它连接到高分子聚合物B上,形成缓释长效药物C如图乙.
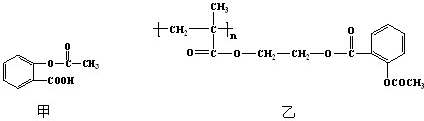
①分子聚合物B的结构简式为


②A与B反应生成C的有机反应类型是
③A可水解成

