摘要:76064708090溶解度/g
网址:http://m.1010jiajiao.com/timu_id_399676[举报]
(2011?惠州模拟)某学习小组通过查阅资料,设计如下方案制备KMnO4:

已知:①3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O
②几种物质的溶解度:
(1)第一步固体熔融时除三脚架、泥三角、细铁棒、坩埚钳外,还需的仪器是
A.酒精灯 B.铁坩埚 C.瓷坩埚 D. 烧杯
(2)反应Ⅰ的化学方程式
(3)反应Ⅱ的条件为电解,其化学方程式为
(4)两个途径中操作a、b相同,均包括
(5)最后可以用1.5mol?L-1的草酸(H2C2O4)溶液滴定KMnO4溶液来测定KMnO4粗品的纯度(质量分数),则还需要采集的数据为
查看习题详情和答案>>

已知:①3MnO2+KClO3+6KOH
| ||
②几种物质的溶解度:
| 温度 | 溶解度/g | ||
| K2CO3 | KOH | KMnO4 | |
| 20℃ | 111 | 112 | 6.38 |
| 60℃ | 127 | 154 | 22.1 |
AB
AB
.A.酒精灯 B.铁坩埚 C.瓷坩埚 D. 烧杯
(2)反应Ⅰ的化学方程式
3K2MnO4+2CO2=MnO2+2KMnO4+2K2CO3
3K2MnO4+2CO2=MnO2+2KMnO4+2K2CO3
;(3)反应Ⅱ的条件为电解,其化学方程式为
2K2MnO4+2H2O
2KOH+2KMnO4+H2↑
| ||
2K2MnO4+2H2O
2KOH+2KMnO4+H2↑
.
| ||
(4)两个途径中操作a、b相同,均包括
蒸发浓缩
蒸发浓缩
、冷却结晶
冷却结晶
、过滤等3步;在整个方案中可以循环利用的产物有KOH、MnO2
KOH、MnO2
.(5)最后可以用1.5mol?L-1的草酸(H2C2O4)溶液滴定KMnO4溶液来测定KMnO4粗品的纯度(质量分数),则还需要采集的数据为
滴定时消耗草酸溶液的体积、KMnO4粗品的质量
滴定时消耗草酸溶液的体积、KMnO4粗品的质量
.要使工业废水中的重金属离子Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+与这些离子形成的化合物的溶解度如表:
|
查看习题详情和答案>>
锂在原子能工业中具有十分独特的地位,被誉为“高能金属”,它推动着能源工业,尤其是电池技术的发展.盐湖卤水中锂的含量较高,资源丰富,提炼锂的价格低廉,成为国内外开发生产锂的主攻方向.把盐湖卤水自然日晒和冷冻,从卤水中析出食盐、泻利盐、钾盐镁矾和光卤石等一系列盐类,得到富含MgC12的浓缩母液,其中LiC1的浓度达10%以上.把浓缩母液经高温炉分解除去MgC12等一系列过程,最终得到金属锂.其主要生产工艺流程如下:
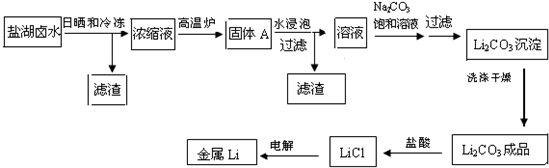
已知:Li2CO3在不同温度的溶解度如下表:
(1)写出浓缩母液在高温炉中分解的化学方程式
(2)写出盐酸与Li2CO3反应的离子方程式
(3)洗涤所得Li2CO3沉淀要用热水而非冷水,原因是
(4)熔融LiCl电解的环境是
查看习题详情和答案>>

已知:Li2CO3在不同温度的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
MgCl2+2H2O=Mg(OH)2+2HCl
MgCl2+2H2O=Mg(OH)2+2HCl
.(2)写出盐酸与Li2CO3反应的离子方程式
Li2CO3+2H+=2Li++CO2↑+H2O
Li2CO3+2H+=2Li++CO2↑+H2O
.(3)洗涤所得Li2CO3沉淀要用热水而非冷水,原因是
Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗
Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗
.(4)熔融LiCl电解的环境是
de
de
a.氢气中 b.氮气中 c.空气中 d.真空中 e.He气.(2010?泰州三模)某化学研究性学习小组通过查阅资料,设计了如图所示的方法来制备KMnO4.
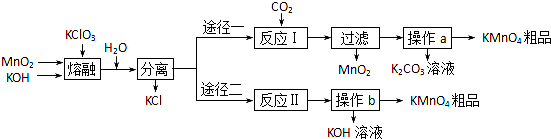
已知:①3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O
②几种物质的溶解度:
请回答下列问题:
(1)第一步固体熔融时除三脚架、泥三角、细铁棒、坩埚钳外,还需下列仪器中的
A.蒸发皿 B.烧杯 C.酒精灯 D.铁坩埚
(2)反应Ⅰ中氧化产物与还原产物的物质的量之比为
(3)反应Ⅱ的条件为电解,写出反应Ⅱ的化学方程式
(4)途径一、二中的操作a、b相同,均包括
(5)通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①实验时要将草酸晶体(H2C2O4?2H2O)配成标准溶液,则配制100mL1.5mol?L-1的草酸溶液,需要称取草酸晶体的质量为
②该实验中除草酸晶体的质量外,还需要采集的数据有
查看习题详情和答案>>

已知:①3MnO2+KClO3+6KOH
| ||
②几种物质的溶解度:
| 温度 | 溶解度/g | ||
| K2CO3 | KOH | KMnO4 | |
| 20℃ | 111 | 112 | 6.38 |
| 60℃ | 127 | 154 | 22.1 |
(1)第一步固体熔融时除三脚架、泥三角、细铁棒、坩埚钳外,还需下列仪器中的
CD
CD
.A.蒸发皿 B.烧杯 C.酒精灯 D.铁坩埚
(2)反应Ⅰ中氧化产物与还原产物的物质的量之比为
2:1
2:1
;该反应中可以循环利用的产物是MnO2
MnO2
.(3)反应Ⅱ的条件为电解,写出反应Ⅱ的化学方程式
2K2MnO4+2H2O
2KOH+2KMnO4+H2↑
| ||
2K2MnO4+2H2O
2KOH+2KMnO4+H2↑
.
| ||
(4)途径一、二中的操作a、b相同,均包括
蒸发浓缩、降温结晶
蒸发浓缩、降温结晶
、过滤等3步.(5)通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数).
①实验时要将草酸晶体(H2C2O4?2H2O)配成标准溶液,则配制100mL1.5mol?L-1的草酸溶液,需要称取草酸晶体的质量为
18.9g
18.9g
.②该实验中除草酸晶体的质量外,还需要采集的数据有
滴定时消耗草酸溶液的体积、KMnO4粗品的质量
滴定时消耗草酸溶液的体积、KMnO4粗品的质量
.