网址:http://m.1010jiajiao.com/timu_id_399672[举报]
(05年江苏卷)已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
A . 3Cl2+6FeI2=2FeCL3+4FeI3
B . Cl2+FeI2=FeCl2+I2
C. Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
D . 2Fe3++2I―=2Fe2++I2
查看习题详情和答案>>(08年江苏卷)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 _____ 。
(2)B的氢化物的分子空间构型是 ______ 。其中心原子采取______ 杂化。
(3)写出化合物AC2的电子式_____ ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 _____ 。
(4)E的核外电子排布式是_____ ,ECl3形成的配合物的化学式为 ___ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是_____ 。
查看习题详情和答案>>(05年全国卷)(15分)已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
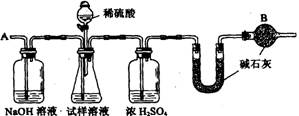
主要实验步骤如下:①按图组装仪器,并检查装置的气密性②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液③称量盛有碱石灰的U型管的质量,得到bg④从分液漏斗滴入6mol?L-1的硫酸,直到不再产生气体时为止⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg;
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明 ;
(2)装置中干燥管B的作用是 ;
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填高、偏低或不变)
(4)步骤⑤的目的是 ;
(5)步骤⑦的目的是 ;
(6)该试样中纯碱的质量分数的计算式为 ;
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验法。
查看习题详情和答案>>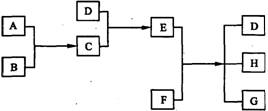 (05年全国卷)(15分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
(05年全国卷)(15分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示: