网址:http://m.1010jiajiao.com/timu_id_399344[举报]
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为
(2)若向达到(1)的平衡体系中充入氩气,则平衡向
(3)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与 (1)的平衡中的X的转化率相比较
A.无法确定 B.一定大于 (1)
C.一定等于 (1)D.一定小于 (1)
(4)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体.甲烷气体燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
356g“可燃冰”(分子式为CH4?9H2O)释放的甲烷气体完全燃烧生成液态水.放出的热量为
(2)某种燃料电池,一个电极通入空气,另一电极通入液化石油气(以C4H10表示),电池的电解质是掺入了Y2O3的ZrO2晶体,它在高温下传导O2-.
已知该电池负极的电极反应为:C4H10+2O2--4e-=CO2+H2O,则该电池正极的电极反应式为
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)?CO2(g)+H2(g)
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:T℃时物质的浓度(mol/L)变化
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
②已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为
③397℃时该反应的平衡常数为12,请判断该反应的△H
(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5mol(L?min);乙:ν(Y)=2mol(L?min);丙:ν(Z)=4.5mol(L?min);丁:ν(X)=0.075mol(L?s).若其他条件相同,温度不同,温度由高到低的顺序是(填序号)
(3)若向达到(1)的平衡体系中充入氮气,则平衡向
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则a、b、c应满足的关系为
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则起始时维持化学反应向逆反应方向进行,则c的取值范围应为
(12分)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应: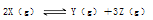
(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为____________mol(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5mol(L·min);乙:ν(Y)=2mol(L·min);丙:ν(Z)=4.5mol(L·min);丁:ν(X)=0.075mol(L·s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)________________。
(3)若向达到(1)的平衡体系中充入氮气,则平衡向___(填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___移动。
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比___
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则a、b、c应满足的关系为____________。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,则起始时维持化学反应向逆反应方向进行,则c的取值范围应为______________。
查看习题详情和答案>>
(14分)丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l);△H=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:
CO (g)+H2O(g)
 CO2(g) +H2 (g)
CO2(g) +H2 (g)
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO )
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
② T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:
|
时间 / min |
CO |
H2O(g) |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
0.100 |
0.200 |
0.100 |
0.100 |
|
4 |
0.100 |
0.200 |
0.100 |
0.100 |
|
5 |
0.116 |
0.216 |
0.084 |
C1 |
|
6 |
0.096 |
0.266 |
0.104 |
C2 |
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的。则第4~5min之间,改变的条件 ,第5~6min之间,改变的条件是 。
已知420℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol/L,则CO在此条件下的转化率为 。又知397℃时该反应的平衡常数为12,请判断该反应的△H 0 (填“>”、“=”、“<”).
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;
燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2—。在电池内部O2—移向_ ___极(填“正”或“负”);电池的负极反应式为 。
(4)用上述燃料电池用惰性电极电解足量Mg(NO3)2和NaCl的混合溶液。电解开始后阴极的现象为____ 。
查看习题详情和答案>>