摘要:②平衡 ③右或正反应 升高温度或减少了水的浓度
网址:http://m.1010jiajiao.com/timu_id_356362[举报]
一定温度下,向一容积为2L的恒容密闭容器中充入2molA与3molB,在一定条件下反应:A(g) +3B(g)![]() xC(g)+yD(g) (x、y为正整数),反应进行2min后达到平衡,已知2min内用C物质的浓度变化量表示的平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知反应速率v(B) : v(C)=3 : 2 ,试计算:
xC(g)+yD(g) (x、y为正整数),反应进行2min后达到平衡,已知2min内用C物质的浓度变化量表示的平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知反应速率v(B) : v(C)=3 : 2 ,试计算:
(1)x、y的值分别分别是 和
(2)平衡时反应物A的转化率
(3)平衡常数K= (可以用分数表示)
查看习题详情和答案>>丙烷在燃烧时能放出大量的热,它是液化石油气的主要成分,作为能源应用于人们的日常生产和生活.
已知:
①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l)△H1=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=
(2)现有1mol C3H8在不足量的氧气里燃烧,生成1mol CO和2mol CO2以及气态水,将所有的产物通入一个固定体积为1L的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H1=+41.2kJ/mol,5min后体系达到平衡,经测定,H2为0.8mol,则v(H2)=
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-.在电池内部O2-由
(4)用上述燃料电池用惰性电极电解足量Mg(NO3)2和NaCl的混合溶液.电解开始后阴极的现象为
查看习题详情和答案>>
已知:
①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l)△H1=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=
-2219.9kJ/mol
-2219.9kJ/mol
.(2)现有1mol C3H8在不足量的氧气里燃烧,生成1mol CO和2mol CO2以及气态水,将所有的产物通入一个固定体积为1L的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H1=+41.2kJ/mol,5min后体系达到平衡,经测定,H2为0.8mol,则v(H2)=
0.16mol/L?min-1
0.16mol/L?min-1
,此过程吸收的热量为32.96kJ
32.96kJ
.(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-.在电池内部O2-由
正
正
极移向负
负
极(填“正”或“负”);电池的负极电极反应式为C3H8+10O2--20e-=3CO2+4H2O
C3H8+10O2--20e-=3CO2+4H2O
.(4)用上述燃料电池用惰性电极电解足量Mg(NO3)2和NaCl的混合溶液.电解开始后阴极的现象为
有无色气体生成,有白色沉淀生成
有无色气体生成,有白色沉淀生成
.向一容积为5L的恒容密闭容器中充入5molA与8molB,在一定条件下反应:2A(g)+3B(g)?xC(g)+yD(g)(x、y为正整数)反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/L?min,D的平衡浓度为0.3mol/L,又知v(B):v(C)=3:2,则下列说法中一定不正确的是( )
查看习题详情和答案>>
哈三中某课外活动小组改进铜与浓硫酸反应的实验,制备并验证二氧化硫的性质,请回答下列问题:
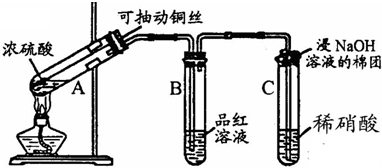
(1)铜丝在实验中的作用:
(2)实验过程中在装置C中会看到什么现象?
(3)已知反应:2SO2(g)+O2(g) 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
A.混合气体密度保持不变
B.c(SO2):c(O2):c(SO3)=2:1:2
C.容器内气体分子总数不随时间变化
D.相同时间内,消耗2n mol SO2的同时消耗n mol O2
(4)将0.23mol SO2和0.11mol O2放入容积为1L的密闭容器中,在一定温度下,经过2min反应达到平衡,得到0.12mol SO3.则用SO2浓度变化来表示反应速率为υ(SO2)=
若此时保持温度不变,同时通入0.12mol SO3和 0.15mol O2,则平衡
但若保持温度不变,只通入1.00mol O2,则重新达到平衡时,SO2的平衡浓度
查看习题详情和答案>>

(1)铜丝在实验中的作用:
控制反应的开始和停止
控制反应的开始和停止
.(2)实验过程中在装置C中会看到什么现象?
生成无色气体并变为红棕色
生成无色气体并变为红棕色
;请用化学方程式解释:SO2+HNO3=H2SO4+NO2NO+02=2NO2
SO2+HNO3=H2SO4+NO2NO+02=2NO2
.(3)已知反应:2SO2(g)+O2(g)
 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是C
C
.A.混合气体密度保持不变
B.c(SO2):c(O2):c(SO3)=2:1:2
C.容器内气体分子总数不随时间变化
D.相同时间内,消耗2n mol SO2的同时消耗n mol O2
(4)将0.23mol SO2和0.11mol O2放入容积为1L的密闭容器中,在一定温度下,经过2min反应达到平衡,得到0.12mol SO3.则用SO2浓度变化来表示反应速率为υ(SO2)=
0.06mol/L?min-1
0.06mol/L?min-1
.若此时保持温度不变,同时通入0.12mol SO3和 0.15mol O2,则平衡
不移动
不移动
(填“正向移动”、“逆向移动”、“不移动”、“无法确定”).但若保持温度不变,只通入1.00mol O2,则重新达到平衡时,SO2的平衡浓度
减小
减小
.(填“填大”、“不变”或“减小”),O2的转化率减小
减小
(填“升高”、“不变”或“降低”),SO2的体积分数减小
减小
(填“增大”、“不变”或“减小”).