网址:http://m.1010jiajiao.com/timu_id_344734[举报]
第Ⅰ卷共21小题,每小题6分,共126分。
一、选择题:选对的给6分,选错或未选的给0分。
1.B 2.A 3.C 4.A 5.D 6.C 7.D 8.B 9.C 10.D 11.D 12.A 13.D
二、选择题:全部选对的得6分,选对但不全的得3分,有选错的得0分。
14.AD 15.BD 16.A 17.B 18.C 19.B 20.AC 21.C
第Ⅱ卷共10小题,共174分。
 22.(18分)
22.(18分)
(1)(6分)在6.122~6.125范围内均可 11.050
(2)(12分)
① 如图所示
② E
3
23.(15分)
(1)夯杆加速上升阶段:
加速度 a =
a =
则夯杆匀加速上升的时间  s = 2 s
s = 2 s
(2)夯杆加速上升的高度  =
= m
=
m
=
在加速上升阶段,电动机对夯杆做的功 W1=2 μ FN h1 = 4.8×104 J
夯杆匀速上升阶段上升高度
h2 = h-h1 =
电动机对夯杆做的功 W2 = mgh2 = 2.4×104J
每个打夯周期中,电动机对夯杆所做的功 W = W1+ W2 = 7.2×104J
评分标准:(1)问6分,(2)问9分,共15分。
24.(19分)
设物体A与B碰前的速度为v1
由动能定理得  ×2mv02-
×2mv02- ×2mv12=2μmg x1
1
×2mv12=2μmg x1
1
物体A与B碰后连接在一起的速度为v2
由动量守恒定律得 2mv1 = 3mv2 2
设物体A、B 一起运动到P点时的速度为v3
由动能定理得  ×3mv22-
×3mv22- ×3mv32=3μmg( x1+2 x2)
3
×3mv32=3μmg( x1+2 x2)
3
从P点运动到圆周轨道最高点的过程中
由机械能守恒定律得  ×3mv32= 3mg×2R+
×3mv32= 3mg×2R+ ×3mv42
4
×3mv42
4
在圆周轨道的最高点 3mg= 5
5
联立以上各式得v0= ≈
≈
评分标准:134式各4分,25式各2分,结果3分,共19分。
25.(20分)
⑴ 从A点射出的粒子,由A到A′的运动时间为T,根据运动轨迹和对称性可得
x轴方向 
y轴方向 
得: 
⑵ 设到C点距离为△y处射出的粒子通过电场后也沿x轴正方向射出,粒子第一次到达x轴用时△t,水平位移为△x,
则 ㄓx= v0ㄓt , 
若满足 ,则从电场射出时的速度方向也将沿x轴正方向
,则从电场射出时的速度方向也将沿x轴正方向
解之得:
即AC间y坐标为 (n = 1,2,3,……)的粒子满足要求。
(n = 1,2,3,……)的粒子满足要求。
评分标准:(1)问6分,(2)问14分,共20分。
26.(14分)
(1)Fe、S
(2)a、d
(3)2Fe3++2I-=== 2Fe2++I2 S2O82 -+2Fe2+=== 2SO42-+2Fe3+
(4)① Al3++4OH -=== AlO2-+2H2O [或Al3++4OH -=== Al(OH)4-]
② 0.8
27.(18分)
(1)Cu CaCO3 Cu(OH)2
 (2) 非极性
(2) 非极性
(3)2Na2O2+2CO2 === 2Na2CO3 + O2↑ CuO + 2H+ === Cu2++H2O
(4)① b、d b ②稀盐酸 a c ③反应器、干燥器 、防倒吸装置等。
28.(13分)
(1)原试剂瓶中盛有的是无色溶液,而这些物质的溶液都是有颜色的
(2)原试剂瓶中盛有的溶液应呈酸性,而二者的水溶液呈中性(或不能使石蕊试液显红色) NH4++H2O NH3?H2O+H+
NH3?H2O+H+
(3)A、B、D Zn+2H+=== Zn2++H2↑
(4)测定溶液的pH,若pH<1,则说明溶质是H2SO4;若pH=1,则说明溶质是NaHSO4或KHSO4,然后可通过焰色反应来进一步确定。或用中和滴定法来对试剂的成分进行确定。(其他答案合理均可)
29. (15分)
(1)①紫色石蕊试液 紫色石蕊试液变红 (其他方法合理均可)
 ②
②
FeCl3溶液 溶液显紫色
 (2)3
(2)3

(3) CH3COO― ―OOCH 或 (其他答案合理均可)
CH3COO― ―OOCH 或 (其他答案合理均可)
(4) 取代反应 还原反应
 O
O
CH3CH2O―  ―NH―C―CH3
―NH―C―CH3
30.(共20分,除标明外每空2分)
(1)①aa ② Aa
(2)① Y染色体的非同源区段 该基因控制的性状只在雄性个体中表现
② 线粒体
③ 7 XaXa×XAYa (或XaXa×XaYA、XAXa×XaYA、XAXa×XAYa) 其他正确答案也得分
(3)①(共4分,答错1空扣1分)
氨基酸序号
162
163
164
165
正常翅密码子
CAU
AUG
GAG
UAU
匙形翅密码子
ACA
UAU
GGA
GUA
②增添
31.(共22分,除标明外每空2分)
(1)生长素是否在光的影响下被分解? 生长素不会在光的影响下被分解。
(2)薄玻璃片分割胚芽鞘是否影响胚芽鞘产生生长素? 薄玻璃片分割胚芽鞘不会影响胚芽鞘产生生长素。
(3)①在单侧光的影响下,向光侧的生长素是否会向背光侧转移?
②见下图。
 |
说明:共6分,其中薄玻璃片2分,画错一项不得分;单侧光每项1分;琼脂块标号2分。
③ α5=α6;α7>α8。
(4)生长素在背光一侧比向光一侧分布多,是因为在单侧光的影响下,向光侧的生长素向背光侧转移,而不是向光侧的生长素在光的影响下被分解。(4分)
B.若在水中加入少量的硫酸钠,电解结束后溶液的pH将会保持不变
C.电解过程中,阴极区附近的溶液的pH会升高
D.当电解产生氧气1.12 L(标准状况)时,转移的电子总数为0.2mol
下列有关水的电解实验的说法中不正确的是( )
A.为提高水的电解速率,可以在水中加入少量的氯化钠
B.若在水中加入少量的硫酸钠,电解结束后溶液的pH将会保持不变
C.电解过程中,阴极区附近的溶液会使酚酞试液变红
D.当电解产生氧气1.12 L(标准状况)时,转移的电子总数为0.2mol
查看习题详情和答案>>2013年10月我市因台风菲特遭受到重大损失,市疾控中心紧急采购消毒药品,以满足灾后需要。复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2是一种无色粘稠液体,请回答下列问题:
(1)下列方程中H2O2所体现的性质与其可以作为消毒剂完全一致的是??????? 。
A.BaO2+2HCl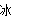 H2O2+BaCl2
H2O2+BaCl2
B.Ag2O+H2O2 =2Ag+O2+H2O???
C.2H2O2 2H2O+O2↑
2H2O+O2↑
D.H2O2+NaCrO2+NaOH=Na2CrO4 +H2O
(2)火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g)? △H= - 534 kJ·mol-1???
H2O2(1)=H2O(1)+1/2O2(g)? △H= - 98.64 kJ·mol-1
H2O(1)=H2O(g)? △H=+44kJ·mol-l
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H=?????????? ,
该反应的△S=??????? 0(填“>”或“<”)。
(3)H2O2是一种不稳定易分解的物质。
①如图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图

②实验证实,往Na2CO3溶液中加入H2O2也会有气泡产生。已知常温时H2CO3的电离常数分别为Kal=4.3×l0-7,Ka2 = 5.0 ×l0-11 。Na2CO3溶液中CO32-第一步水解常数表达式Khl=????? ,常温时Khl的值为??????????? 。若在Na2CO3溶液中同时加入少量Na2CO3固体与适当升高溶液温度,则Khl的值
?????????? (填变大、变小、不变或不确定)。
(4)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。

注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L-l的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是????????????????? (填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低??????
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢?????
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小
查看习题详情和答案>>
2013年10月我市因台风菲特遭受到重大损失,市疾控中心紧急采购消毒药品,以满足灾后需要。复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2是一种无色粘稠液体,请回答下列问题:
(1)下列方程中H2O2所体现的性质与其可以作为消毒剂完全一致的是 。
A.BaO2+2HCl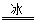 H2O2+BaCl2
H2O2+BaCl2
B.Ag2O+H2O2 =2Ag+O2+H2O
C.2H2O2 2H2O+O2↑
2H2O+O2↑
D.H2O2+NaCrO2+NaOH=Na2CrO4 +H2O
(2)火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g) △H=" -" 534 kJ·mol-1
H2O2(1)=H2O(1)+1/2O2(g) △H=" -" 98.64 kJ·mol-1
H2O(1)=H2O(g) △H=+44kJ·mol-l
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H= ,
该反应的△S= 0(填“>”或“<”)。
(3)H2O2是一种不稳定易分解的物质。
①如图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图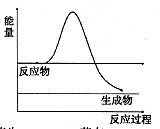
②实验证实,往Na2CO3溶液中加入H2O2也会有气泡产生。已知常温时H2CO3的电离常数分别为Kal=4.3×l0-7,Ka2 =" 5.0" ×l0-11 。Na2CO3溶液中CO32-第一步水解常数表达式Khl= ,常温时Khl的值为 。若在Na2CO3溶液中同时加入少量Na2CO3固体与适当升高溶液温度,则Khl的值
(填变大、变小、不变或不确定)。
(4)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。
注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L-l的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是 (填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小
(1)下列方程中H2O2所体现的性质与其可以作为消毒剂完全一致的是 。
A.BaO2+2HCl
 H2O2+BaCl2
H2O2+BaCl2B.Ag2O+H2O2 =2Ag+O2+H2O
C.2H2O2
 2H2O+O2↑
2H2O+O2↑D.H2O2+NaCrO2+NaOH=Na2CrO4 +H2O
(2)火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g) △H=" -" 534 kJ·mol-1
H2O2(1)=H2O(1)+1/2O2(g) △H=" -" 98.64 kJ·mol-1
H2O(1)=H2O(g) △H=+44kJ·mol-l
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H= ,
该反应的△S= 0(填“>”或“<”)。
(3)H2O2是一种不稳定易分解的物质。
①如图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图

②实验证实,往Na2CO3溶液中加入H2O2也会有气泡产生。已知常温时H2CO3的电离常数分别为Kal=4.3×l0-7,Ka2 =" 5.0" ×l0-11 。Na2CO3溶液中CO32-第一步水解常数表达式Khl= ,常温时Khl的值为 。若在Na2CO3溶液中同时加入少量Na2CO3固体与适当升高溶液温度,则Khl的值
(填变大、变小、不变或不确定)。
(4)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。

注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L-l的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是 (填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小