网址:http://m.1010jiajiao.com/timu_id_317240[举报]
A卷
1.C 2.B 3.C 4.B 5.B 6.C 7.B 8.A 9.B 10.A 11.A 12.C 13.C 14.B 15.B
16. ①Fe3++3H2O Fe(OH)3+3H+
②2Fe3++Fe=3Fe2+
③Fe3++SCN…=[Fe(SCN)]2+
Fe(OH)3+3H+
②2Fe3++Fe=3Fe2+
③Fe3++SCN…=[Fe(SCN)]2+
④Fe3++3NH3?H2O=Fe(OH)3+3NH4+ ⑤2Fe3++H2S=2Fe2++S↓+2H+(每个2分)
17. CH3OCH3+16OH--12e-=2CO32 -+11H2O;3O2+6H2O+12e-===12OH-;CH3OCH3+4OH-+3O2=2CO32 -+5H2O(每个2分)
18. (1)① Mg2+、SO42−、H+ ②Ba2+、NO3−、OH−;(全对给2分,答不全但答到H+ 或OH−得1分)
19. (1)0.2 mol(1分)(2)SO2、NO2(1分) (3)AC(全对给2分,答不全得1分)
20. (1)H2(1分)(2)①Fe+2H+=Fe2++H2↑②AlO2-+4H+=Al3++2H2O
③4Fe2++8NH3?H2O+O2+2H2O=4Fe(OH)3↓+8NH4+或:Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+、 4Fe(OH)2+O2+2H2O=4Fe(OH)3(每个2分)
(3) Al3+和Na+(全对给2分,答不全得1分) (4) H2SO4、HNO3(全对给2分,不全得1分)
21. (1)ECDBAGF(2分);酚酞(1分);无色变为浅红色(或粉红色)且半分钟不褪去(2分);
(2)偏大(1分)(3)100.00mL容量瓶(1分)(4)偏小 偏小 偏大(每个1分)
(5)4.20mol/L(2分)
22. (1) 7g;8g;(2) 3.5mol/L
B卷
B卷:23.C 24.D 25.C 26.B 27.B 28.C 29.D 30.C
31.(1)3.6 mol (2)≥0(说明:答“任意值”可得分)(3)3.6 mol< n(SO3)≤4 mol(每个2分)
32. (1)NH4C1、① ;(2)NH4Cl和NH3?H2O(答NH4Cl和NH3也给分);NH4Cl和HCl;
(3)小于 大于;(每个1分)
33. (1)将Fe3+ 还原为Fe2+;析出(或分离、或得到)FeSO4?7H2O;(每个2分)
(2) FeSO4?7H2O 石灰(或碳酸钙、废碱);(每个1分)
 (3)TiO2+2C+2Cl2 TiCl4+2CO(2分);CO(1分);①TiCl4+2Mg△ㄔㄔTi+2MgCl2(2分);②防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用(2分)③加入足量盐酸,除去金属镁,过滤,并用蒸馏水洗涤固体得金属钛。(2分)
(3)TiO2+2C+2Cl2 TiCl4+2CO(2分);CO(1分);①TiCl4+2Mg△ㄔㄔTi+2MgCl2(2分);②防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用(2分)③加入足量盐酸,除去金属镁,过滤,并用蒸馏水洗涤固体得金属钛。(2分)
34. (1)0.6 mol/L (2分);(2)97.5mL(2分);(3)35mL(3分)

图1-5
(1)Ti的原子序数为22,Ti位于元素周期表中第_________周期,第________族。
(2)步骤①加Fe的目的是:__________________________________________________;
步骤②冷却的目的是:_____________________________________________________。
(3)上述制备TiO2的过程中,可以利用的副产物是______________________;考虑成本和废物综合利用因素,废液中应加入_________处理。
(4)由金红石(TiO2)制取单质Ti,涉及的步骤为:
![]()
已知:①C(S)+O2(g)![]() CO2(g);ΔH=-393.5 kJ·mol-1
CO2(g);ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)![]() 2CO2(g);ΔH=-566 kJ·mol-1
2CO2(g);ΔH=-566 kJ·mol-1
③TiO2(S)+2Cl2(g)![]() TiCl4(s)+O2(g);ΔH=+141 kJ·mol-1
TiCl4(s)+O2(g);ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)![]() TiCl4(s)+2CO(g)的ΔH=______________。
TiCl4(s)+2CO(g)的ΔH=______________。
反应TiCl4+2Mg![]() 2MgCl2+Ti在Ar气氛中进行的理由是_______________________。
2MgCl2+Ti在Ar气氛中进行的理由是_______________________。
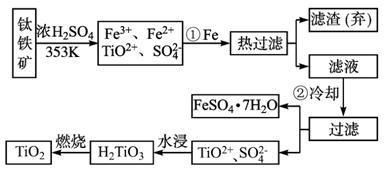
图2-3-3
(1)Ti的原子序数为22,Ti位于元素周期表中第_________周期,第_________族。
(2)步骤①加Fe的目的是:_____________________________________________;
步骤②冷却的目的是:________________________________________________。
(3)上述制备TiO2的过程中,可以利用的副产物是_________;考虑成本和废物综合利用因素,废液中应加入_________处理。
(4)由金红石(TiO2)制取单质Ti,涉及的步骤为:
![]()
已知:①C(s)+O2(g)====CO2(g); ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)====2CO2(g); ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)====TiCl4(s)+O2(g); ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)====TiCl4(s)+2CO(g)的ΔH=_________。
反应TiCl4+2Mg====2MgCl2+Ti在Ar气氛中进行的理由是____________________________。
查看习题详情和答案>>
(1)Ti的原子序数为22,Ti位于元素周期表中第_________周期,第_________族。
(2)步骤①加Fe的目的是___________________________;
步骤②冷却的目的________________________________。
(3)上述制备TiO2的过程中,可以利用的副产物是_________,考虑成本和废物综合利用因素,废液中应加入_________处理。
(4)由金红石(TiO2)制取单质Ti,涉及到的步骤为:
TiO2![]() TiCl4
TiCl4![]() Ti
Ti
已知:①C(s)+O2(g)====CO2(g);ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g)====2CO2(g);ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)====TiCl4(s)+O2(g);ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)====TiCl4(s)+2CO(g)的ΔH=__________。
反应TiCl4+2Mg====2MgCl2+Ti在Ar气氛中进行的理由是____________________。
查看习题详情和答案>>钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前最好的白色颜料。制备TiO2、TiCl4和Ti的原料是钛铁矿,我国的钛铁矿储量居世界首位。用含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取TiO2、TiCl4和Ti的流程如下:
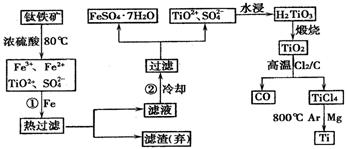
(1) Fe的原子序数为26,Fe位于元素周期表中第 周期,第 族
(2) 步骤①加铁粉的目的是
步骤②冷却的目的是
(3) 上述过程中,可以利用的副产物是
(4) 写出TiO2、Cl2、C在高温下发生反应的化学方程式
(5) 反应TiCl4+2Mg![]() 2MgCl2+Ti , 在Ar气体中进行的目的是
2MgCl2+Ti , 在Ar气体中进行的目的是
钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:
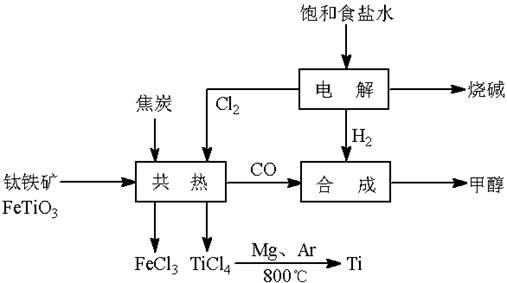
(1)电解饱和食盐水时,阳极的电极反应为 。
(2)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式________________________。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s);△H = – 641 kJ/mol
![]() ②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s);△H= 。
![]() 反应2Mg(s) + TiCl4(s)
反应2Mg(s) + TiCl4(s)![]() 2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是 。
(4)在上述产业链中,合成96 t 甲醇理论上消耗H2 t (不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH + 3O2 + 4OH-=2CO32- + 6H2O。该燃料电池发生反应时正极区溶液的pH (填“增大”、“减小”或“不变”),该电池中负极上的电极反应是________________________________________________。
查看习题详情和答案>>