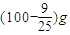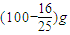摘要:30℃时.硫酸铜的溶解度为25g.所以析出晶体后.饱和溶液中溶质和溶剂的质量比为25∶100.所以.</PGN0040.TXT/PGN>g∶g=100∶25解出y=154g解法2 析晶前溶质质量为110g.析出晶体质量为y.溶液中溶质质量为g.饱和溶液的质量为g.所以∶25=g∶g解出y=154 g解法3 用守恒法.原溶液中溶质质量=析晶后饱和溶液中溶质质量+晶体中的溶质质量.设析出xg胆矾.其中硫酸铜的质量为16x/25.结晶水的质量为9x/25.蒸发水和冷却后.溶液中溶剂的质量为100-9x/25.根据30℃硫酸铜的溶解度可知:晶后溶质的质量:溶剂质量=25∶100.所以溶质质量=[25÷100]g.原饱和溶液溶质的质量110g=16x/25g+[25÷100]g解出x=154g解法4 设析出胆矾的质量为x余下的饱和溶液质量∶余下溶质质量=∶S余下饱和溶液的质量为310-100-x.余下溶质为110-16x/25.=125∶25解x=154g[小结]回答很好.下面我们将解题思路归纳如下:有关溶解度计算的常用公式有:①某温度下.饱和溶液中溶质的质量分数=(饱和溶液中溶质质量/饱和溶液质量)×100%=S/×100%②某温度下.饱和溶液中溶质质量:溶剂质量=S∶100溶质质量∶饱和溶液质量=S∶100+S③一定温度下的饱和溶液蒸发一部分水.再冷却至原来的温度.将有晶体析出.析出晶体后余下的溶液仍为饱和溶液.若将析出的晶体与蒸发的水重新混合.也应得到饱和溶液.若晶体中不含结晶水.则:蒸发的水的质量∶析出的晶体的质量=100∶S若晶体中含结晶水.则由于析出含结晶水的晶体后的溶液仍为饱和溶液.所以蒸发的水和析出的结晶水与析出的晶体中的无水物混合在一起也可配成饱和溶液.所以.析出的晶体中的无水物的质量∶(结晶水的质量+蒸发水的质量)=S∶100④将饱和溶液从高温冷却至低温.由于一般来说.其溶解度降低.所以将有晶体析出.若晶体中不含结晶水.其质量可用以下2个公式来求:若用100g水在高温下配制饱和溶液.此时可得g饱和溶液.若将饱和溶液降至某温度时.析出的晶体的质量为两个温度下的溶解度之差.所以:析出晶体的质量∶饱和溶液中溶剂的质量=∶100析出晶体的质量∶高温下饱和溶液质量=∶上述公式应根据不同情况加以应用.而解题的基本方法是比例式法或守恒法. 精选题
网址:http://m.1010jiajiao.com/timu_id_233594[举报]
在25℃时,硫酸铜的溶解度为S g,在该温度下,把S克无水硫酸铜粉末加入(100+S)克饱和硫酸铜溶液中,得到一定量的蓝色晶体.若将此蓝色晶体溶解成饱和溶液,应加水的质量是( )
已知25 ℃时,硫酸铜的溶解度为25 g,若将此温度下50 g CuSO4放入100 g水中,充分搅拌溶解后,所得溶液的质量为
A.104.5 g B.111 g C.150 g D.无法计算
查看习题详情和答案>>