网址:http://m.1010jiajiao.com/timu_id_179140[举报]
一、二(63分)
题序
1
2
3
4
5
6
7
8
9
答案
D
B
B
C
B
D
A
C
D
题序
10
11
12
13
14
15
16
17
18
答案
C
D
AD
B
CD
B
A
AC
BD
三、(本题包括2小题,共27分)
19、(11分)(1)搅拌、加热(2分)(2)坩埚钳(1分),用玻璃棒不断搅拌滤液(1分)(3)NaCl(2分)
 (4)稀释溶液,防止降温过程中NaCl析出,提高产品纯度(3分)(5)重结晶(2分)。
(4)稀释溶液,防止降温过程中NaCl析出,提高产品纯度(3分)(5)重结晶(2分)。
20(16分)(1)引流作用(1分) (2) 2H2O2 == 2H2O + O2↑(3分) (3) 炭(或碳、或C) (2分)
(4)(一)[判断猜想]:猜想I不成立 (1分)
(二)[验证(操作)过程]:取少量滤液逐滴滴入稀氨水 (3分)
[实验现象]:先有白色沉淀、滴入过量稀氨水后白色沉淀溶解(3分);
[判断猜想]:结论:主要为氯化锌,其中含少量的氯化铵(3分)。
[若说成氯化铵和氯化锌的混合物给1分;若说成只有氯化锌没有氯化铵0分]
四、(本题包括3小题,共40分)
(3)B、C; (3分,若只选一个对的得1分,全对得3分)
(4)设3min―4min达到平衡时CO、H2 O的平衡浓度为c3, 则CO2 、H2的平衡浓度分别为0.200-c3和0.300- c3
根据: K= (2分)
(2分)
c3=0.120 mol/L (2分,写0.12的不给分) ;
22(12分)(1)Fe(OH)3(2分) (2)氨水 (2分) 不会引入新的杂质(1分)
(3)2Fe3++3Mg(OH)2 == 3 Mg2+ +2Fe(OH)3 (3分)
(4)A C D E (4分)(选对1个给1分,选错1个倒扣1分,但不出现负分。)
23(15分)(1)113~
(5)H2S(g) = H2(g) + S(s) △H = +112.2KJ/mol (3分) (6) 硒 (2分) 氧气 (2分)
五、(本题包括1小题,共10分)
24.(10分)(1)小(1分)(2)CH2=CH2 + H2O → CH3CH2OH (1分)100%(1分)
(3)D E(共2分)(4)①3(2分)
③BCD(2分,漏1个扣1分,漏2个和错选均为0分)
六、(本题包括2小题,每小题10分。考生只能选做一题。26题为“有机化学基础”内容试题,27小题为“物质结构”内容试题)
25 (10分)(1)[根据答到的要点或关键词给分]
①在此条件下,卤代烃的消去反应和取代反应同时进行(1分),有利于消去反应(1分)。
②在此条件下,有利于生成对称烯烃(1分),且卤原子半径越大(1分)越有利于生成对称烯烃(1分)。
若回答只是数据翻译,如:消去(取代)产物比例较大(小),或消去反应谁的比例大、谁的比例小,说出一点给1分,说出几点都如此最多给2分。
 |
⑵① (1分) CH3C≡CH (1分)
 |
|||
 |
|||
26.(10分)
(1) 3d84s2 (2分) ,分子晶体(1分), CO(1分)。
(2) B C (2分) (3)20 (2分) (4)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果。某兴趣小组通过实验研究MnO2的性质![]()
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 。
A、把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B、把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C、把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D、把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验。
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
该小组从上述对比实验中,可以得出的结论是 。
写出在酸性条件下,MnO2氧化I-的离子方程式 。
(3)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1g/cm3)配制浓度3%的H2O2溶液(密度近似为1g/cm3)100mL。其配制方法是:用量筒量取 mL30%H2O2溶液放入 (填仪器名称)中,再加入一定量的水,搅拌均匀。
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡。该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用。请设计一个简单实验证明该假设是否正确。
。
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是 (填序号)。

![]()
A B C D
(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为 。
查看习题详情和答案>>下列实验设计能够成功的是
| 实验目的 | 实验步骤及现象 | |
| A | 检验亚硫酸钠试样是否变质 | 试样  白色沉淀 白色沉淀 沉淀不溶 沉淀不溶 |
| B | 检验某卤代烃是否是氯代烃 | 试样 冷却 冷却  出现白色沉淀 出现白色沉淀 |
| C | 证明酸性条件下H2O2氧化性比I2强 | NaI溶液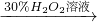 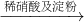 溶液变蓝色 溶液变蓝色 |
| D | 证明Ksp(BaSO4)>Ksp(BaCO3) | BaSO4悬浊液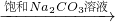 过滤、洗涤得固体 过滤、洗涤得固体 气体 气体 |
- A.A
- B.B
- C.C
- D.D
| 实验目的 | 实验步骤及现象 | |
| A | 检验亚硫酸钠试样是否变质 | 试样 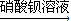 白色沉淀 白色沉淀 沉淀不溶 沉淀不溶 |
| B | 检验某卤代烃是否是氯代烃 | 试样 冷却 冷却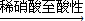 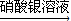 出现白色沉淀 出现白色沉淀 |
| C | 证明酸性条件下H2O2氧化性比I2强 | NaI溶液  溶液变蓝色 溶液变蓝色 |
| D | 证明Ksp(BaSO4)>Ksp(BaCO3) | BaSO4悬浊液 过滤、洗涤得固体 过滤、洗涤得固体 气体 气体 |
A.A
B.B
C.C
D.D
查看习题详情和答案>>
下列实验设计能够成功的是( )
|



