网址:http://m.1010jiajiao.com/timu_id_139895[举报]
生物答案:
1B 2A 3C 4A 5D
30.
Ⅰ.(12分)
⑴
①等量生理盐水。(2分)
③取出标本,在1号中加入适量生理盐水稀释的有机磷农药,2号滴加等量生理盐水(2分)
④同时给两个标本施加相同的电刺激(2分)
振颤不止(或持续收缩)(2分)
正常收缩并及时舒张(2分)
⑵肌肉不收缩或无变化(2分)
Ⅱ.(10分)
⑴糖类、脂肪(2分) ③(2分) 胰岛素(2分)
⑵基因突变(2分) 核糖体、内质网、高尔基体、线粒体(2分)
31.
Ⅰ.(10分)
(1)B(2分) B→D→A→C(2分) 11.3%(2分)(2)水中的溶解氧 (2分)
控制污染物的排放,(1分) 避免过量捕捞。(1分)(其它正确答案正确给分)
Ⅱ.(10分)
⑴X(2分) 隐(2分)
⑵bbXaXa(2分) 7/12 (2分)
⑶ Ⅱ2 Ⅱ3 Ⅲ1 Ⅲ2(2分)
化学答案:
6.D7.C8.C 9.B 10.D 11.C12.A13.B
26.(14分,每空2分)
(1)分子
(2)①非极性 ②镁条在二氧化碳中剧烈燃烧,生成白色粉末,在瓶的内壁有黑色固体附着
(3)电解法
(4)高温常压催化剂
27.(14分,每空2分)(1)①2OH-+CO2==CO32-+H2O ② AC
(2)①c(Na+)>c(AlO2-)>c(OH-)>c(H+) ②Al3++3AlO2-+6H2O==4Al(OH)3↓
(3)①2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
②离子键和极性键(或共价键)
③用湿润的红色石蕊试纸,若变蓝则证明为氨气
28.(16分)(一)(1)28.0 C (各1分)
(2)蒸发皿 5.8或5.9 100 mL容量瓶 (各1分)
(二)(1)能 (1分) (2)⑤和⑥ (1分) ①和⑥ (1分)
4Fe(OH)2+O2+2H2O==4Fe(OH)3(2分)
(3)3Fe2++4H++NO3―==3Fe3++NO↑+2H2O
2Fe2++2H++H2O2==2Fe3++2H2O
2Fe2++4OH一+H2O2==2Fe(OH)3↓(以上任写两组)(4分)
(4)② 几枚铁钉(2分)
29.(16分)
(1)C10H10O4 (2分) (2)羧基(2分) a、c (2分)
(3) (2分)
(2分)
(4)
(2分)酯化反应(1分)
(5)3 (1分) (2分)
物理答案:
14、AC 15、BC 16、A 17、CD 18、D 19、C 20、D 21、A
22、(1)BC 3分 (2)dacb 3分 (3)A 3分
(4)I、共6分 分压2分 测量4分
II、3分
23、(16分)解:把小球斜抛看成反向平抛:
2分
2分
2分 vx=10m/s vy=5m/s
2分
Mv-mvx=0 3分 v=1m/s
W= 3分
W=675J 2分
24、(16分)(1)电场对电子做负功,由动能定理
4分 2分
(2)在nT一(n+1)T的时间内,剪半周期电子减速通过输入腔,射出的速度为v1
4分
1分
后半周期电子加速通过输入腔,射出的速度为v2,
4分
解得 1分 3分
25、(20分)解:⑴做直线运动有: 2分
做圆周运动有: 2分
只有电场时,粒子做类平抛,有:
3分
解得: 粒子速度大小为:
速度方向与x轴夹角为: 2分
粒子与x轴的距离为: 2分
⑵撤电场加上磁场后,有: 解得: 2分
粒子运动轨迹如图所示,圆心C位于与速度v方向垂直的直线上,该直线与x轴和y轴的夹角均为π/4,有几何关系得C点坐标为:
过C作x轴的垂线,在ΔCDM中:
解得: 5分
M点横坐标为: 2分
(4分)(1)同素异形体相互转化的反应热相当小而且转化速率很慢,有时还很不完全,测定反应热有时很困难,因此常用盖斯定律进行计算得到相应数据。已知:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+![]() O2(g)=
O2(g)=![]() P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为____________________。
(2)已知:① C(s)+O2(g)=CO2(g); DH=—393.5kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g); DH=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); DH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH= 。
查看习题详情和答案>>
(4分)(1)同素异形体相互转化的反应热相当小而且转化速率很慢,有时还很不完全,测定反应热有时很困难,因此常用盖斯定律进行计算得到相应数据。已知:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+ O2(g)=
O2(g)=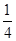 P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为____________________。
(2)已知:① C(s)+O2(g)=CO2(g); DH=—393.5 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g); DH=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); DH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH= 。
(4分)(1)同素异形体相互转化的反应热相当小而且转化速率很慢,有时还很不完全,测定反应热有时很困难,因此常用盖斯定律进行计算得到相应数据。已知:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为____________________。
(2)已知:① C(s)+O2(g)=CO2(g); DH=—393.5 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g); DH=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); DH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH= 。
查看习题详情和答案>>
① C(s)+O2(g)=CO2(g);△H=-393.5kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g);△H=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);△H=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=_____________。
(2)已知298K时下列反应的焓变为
① CH3COOH(l)+2O2(g) = 2CO2(g)+2H2O(l) △H1(298K)= -870.3kJ·mol-1
② C(s)+O2(g) = CO2(g) △H2(298K)= -393.5kJ·mol-1
③ H2(g) +1/2O2(g) = H2O(l) △H3(298K) = -285.8kJ·mol-1
计算在此温度下2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应焓变。△H=_____________。
(3)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式_____________________。
(1)同素异形体相互转化的反应热相当小而且转化速率很慢,有时还很不完全,测定反应热有时很困难,因此常用盖斯定律进行计算得到相应数据。已知:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+![]() O2(g)=
O2(g)=![]() P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为____________________。
(2)已知:① C(s)+O2(g)=CO2(g); DH=—393.5 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g); DH=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g); DH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH= 。
查看习题详情和答案>>