网址:http://m.1010jiajiao.com/timu_id_139546[举报]
一、 选择题(每题2分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
D
B
C
A
B
C
C
B
C
A
C
C
D
题号
14
15
16
17
18
19
20
21
22
23
24
25
答案
A
C
D
D
D
A
D
D
A
D
A
C
二、填空题(本题包括6小题,共计30分)
26. O2+2H2O+4e-=4OH- (1分) 略 (2分)
27. ⑦③⑨①②④⑧⑥⑤ (2分)
28. n-1 (2分)
29.(1)其它离子也沉淀 (1分)
(2)把Fe2+氧化成Fe3+ ;(1分) 增大;(1分) 不妥(1分)引入了钠离子(1分)
(3)BC (2分) (4)CD (2分)
30.(1) 124.24. (1分) (2)2×10-7 mol?L-1; (1分)
(3)> (1分) HCO3-CO32-+H+
HCO3-+H2OH2CO3+OH-、HCO3-的水解程度大于电离程度 (2分)
31.(1)Y (1分) a和c (1分)
(2)0.04 mol?L-1min ; (1分)Kb=(mol?L-1)-1(或mol-1?L); (1分)= (1分)
(3)a,b C(2分) (4)C (2分)
三.实验题(8分)
32. I.无色变红色且半分钟不褪去 (1分) C (1分)
II(1)2MnO4-+10Fe2++16H+=2Mn2++10Fe3++8H2O;(2分)(2) 0.8 mol (2分) (3) AD(2分)
四、计算题(12分)
33、(1)2CuSO4+2H2O=2Cu+O2+2H2SO4 (2分)(2)1.4;(1分) 2:1 (1分)(3)5(2分)
34、(1)消耗的O2物质的量: (1分)
生成的SO3物质的量:
SO2和SO3的物质的量和:
反应前的SO2物质的量: (2分)
SO2的转化率: (1分)
(2)在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量 (2分)
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)  CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH3CH=CH2(g) CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3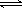 HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)
HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)
(3)在1 L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为 ×100%
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)
 CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1CH3CH=CH2(g)
 CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1 则相同条件下,反应C3H8(g)
 CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)
HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)(3)在1 L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为 ×100%
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)
 CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH3CH=CH2(g) CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5
mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3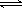 HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)
HCO3-+H+的电离平衡常数Ka1= 。(已知:10-5.60=2.5×10-6)
(3)在1 L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为 ×100%
查看习题详情和答案>>
(1)丙烷脱氢可得丙烯.
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ?mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ?mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H= kJ?mol-1.
(2)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的电离平衡常数Ka1= .(已知:10-5.60=2.5×10-6)
(3)在1L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为 ×100% 查看习题详情和答案>>
(1)丙烷脱氢可得丙烯.
已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ?mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ?mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)的△H=
(2)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的电离平衡常数Ka1=
(3)在1L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为