摘要: (1)防倒吸,(2)C6H5ONa + H2O + CO2 → C6H5OH + NaHCO3 溶液又变澄清(3)有白色沉淀生成 Al3+ + 3NH3?H2O=Al(OH) 3↓ + 3NH4+
网址:http://m.1010jiajiao.com/timu_id_139502[举报]
如图为苯和溴取代反应的改进实验装置.其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑.

填写下列空白:?
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):
 ,该反应的类型为
,该反应的类型为
(2)试管C中苯的作用是
(3)在上述整套装置中,具有防倒吸作用的仪器有
(4)实验结束后,得到粗溴苯要用如下操作提纯,①蒸馏;②水洗;③用干燥剂干燥;④用10% NaOH溶液洗;⑤分液.正确的操作顺序是
A.⑤④②①③B.④②⑤③①C.④②⑤①③D.④⑤③①②
查看习题详情和答案>>

填写下列空白:?
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):


取代
取代
反应.(2)试管C中苯的作用是
除去HBr中混有的溴蒸气
除去HBr中混有的溴蒸气
;反应开始后,观察D试管,看到的现象为石蕊试液变红
石蕊试液变红
;能说明苯与溴发生的是取代反应而不是加成反应的现象为E管中出现浅黄色沉淀
E管中出现浅黄色沉淀
.(3)在上述整套装置中,具有防倒吸作用的仪器有
DEF
DEF
(填字母).(4)实验结束后,得到粗溴苯要用如下操作提纯,①蒸馏;②水洗;③用干燥剂干燥;④用10% NaOH溶液洗;⑤分液.正确的操作顺序是
B
B
A.⑤④②①③B.④②⑤③①C.④②⑤①③D.④⑤③①②
某校化学研究性学习小组为探究Cu(OH)2受热分解产物及产物性质设计如下实验过程:
(1)取0.98g Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示,产物A、B的化学式分别为 和Cu2O.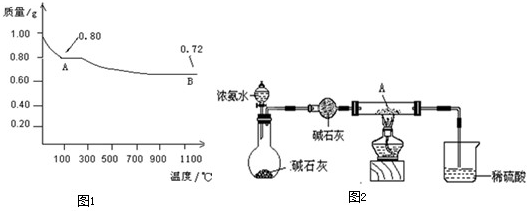
(2)为探究产物A能否被NH3还原设计如图2实验装置(夹持及尾气处理装置未画出)实验中观察到A变成红色物质,同时生成一种无污染的气体,该气体的化学式为 .有人认为在装A物质的试管与烧杯之间需加一个防倒吸装置,你认为是否有必要 ,(填“有”或“没有”)原因是 .
(3)取少量产物B加入足量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,该反应的离子方程式为 .
(4)通过以上实验可以判断出A与B的稳定性大小的结论是:高温时 ;在酸性溶液中 .(用A、B的化学式表示).
查看习题详情和答案>>
(1)取0.98g Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示,产物A、B的化学式分别为

(2)为探究产物A能否被NH3还原设计如图2实验装置(夹持及尾气处理装置未画出)实验中观察到A变成红色物质,同时生成一种无污染的气体,该气体的化学式为
(3)取少量产物B加入足量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,该反应的离子方程式为
(4)通过以上实验可以判断出A与B的稳定性大小的结论是:高温时
(2012?石景山区一模)某校两个班的化学研究性学习小组,在学习了铜和浓硫酸的反应后分别探究足量的锌与浓硫酸反应的过程.一班小组设计了下图装置:

试回答:
(1)请从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
(2)D、E两支试管中CCl4的作用是
(3)本实验能证明浓硫酸具有强氧化性的实验现象为
(4)D中出现浑浊的离子方程式为
(5)某学生注意观察到:实验开始后,C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中出现浑浊;反应一段时间后,C、D、E中的气泡量又会明显增加.请用化学方程式表示“反应一段时间后气泡量又会明显增加”的原因是
二班小组设计了下图装置:

(6)分析出二班小组的设计意图是
(7)装置B中的药品是
(8)能证明产生SO2和H2先后顺序的实验现象是
查看习题详情和答案>>

试回答:
(1)请从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接
3(或4),4(或3)接b,
3(或4),4(或3)接b,
c接2,1
c接2,1
接d(用序号表示).(2)D、E两支试管中CCl4的作用是
防倒吸
防倒吸
.(3)本实验能证明浓硫酸具有强氧化性的实验现象为
C中品红溶液褪色
C中品红溶液褪色
.(4)D中出现浑浊的离子方程式为
Ca2++2OH-+SO2═CaSO3↓+H2O
Ca2++2OH-+SO2═CaSO3↓+H2O
.(5)某学生注意观察到:实验开始后,C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中出现浑浊;反应一段时间后,C、D、E中的气泡量又会明显增加.请用化学方程式表示“反应一段时间后气泡量又会明显增加”的原因是
Zn+H2SO4(稀)═ZnSO4+H2↑
Zn+H2SO4(稀)═ZnSO4+H2↑
.二班小组设计了下图装置:

(6)分析出二班小组的设计意图是
验证产物中先产生水、SO2,后产生H2
验证产物中先产生水、SO2,后产生H2
.(7)装置B中的药品是
无水CuSO4
无水CuSO4
.(8)能证明产生SO2和H2先后顺序的实验现象是
C中品红褪色,D中酸性高锰酸钾不再褪色后,F中有红色物质生成,G中无水硫酸铜变蓝
C中品红褪色,D中酸性高锰酸钾不再褪色后,F中有红色物质生成,G中无水硫酸铜变蓝
.(2011?德州一模)在实验室中用下列装置进行有关实验探究.请回答下列问题:
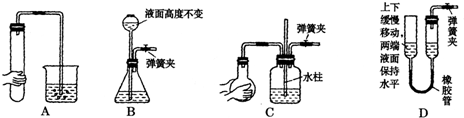
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是
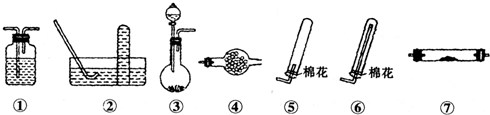
Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是
Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:
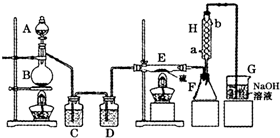
(1)B中反应的离子方程式:
(2)H中冷水的方向为
(3)为了提高S2Cl2的纯度,关键的操作是控制好温度和
(4)尾气处理装置存在明显的缺陷,如何改正:
查看习题详情和答案>>
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是
D
D
.
Ⅱ.若用下列装置③制取并收集干燥的NH3,烧瓶内装的试剂是
生石灰
生石灰
.收集装置应选择⑥
⑥
(填装置序号).证明氨气已收集满的操作是将湿润的红色石蕊试纸靠近瓶口,试纸变蓝(或将蘸有浓盐酸的玻璃棒靠近瓶口,有白烟生成)
将湿润的红色石蕊试纸靠近瓶口,试纸变蓝(或将蘸有浓盐酸的玻璃棒靠近瓶口,有白烟生成)
.
Ⅲ.二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品.
②有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 沸点℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2Cl2 | -77 | 137 | 遇水生成HCl,SO2,S;300℃以上完全分解; S2Cl2+Cl2
|

(1)B中反应的离子方程式:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
(2)H中冷水的方向为
a
a
进b
b
出.(3)为了提高S2Cl2的纯度,关键的操作是控制好温度和
控制浓盐酸的滴速不要过快
控制浓盐酸的滴速不要过快
.(4)尾气处理装置存在明显的缺陷,如何改正:
在G和H之间增加干燥装置;G中加防倒吸装置
在G和H之间增加干燥装置;G中加防倒吸装置
.已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2
2MgO+C).用如图所示的装置进行Mg和SO2的实验:
(1)选择制取SO2的合适试剂
(2)写出装置B中发生的主要反应的化学方程式:
(3)你认为该装置是否有不足之处?
查看习题详情和答案>>
| ||

(1)选择制取SO2的合适试剂
②③
②③
.①10%的H2SO4溶液;②80%的H2SO4溶液; ③Na2SO3固体;④CaSO3固体(2)写出装置B中发生的主要反应的化学方程式:
3Mg+SO2
2MgO+MgS(或写成2Mg+SO2
2MgO+S、Mg+S
MgS)
| ||
| ||
| ||
3Mg+SO2
2MgO+MgS(或写成2Mg+SO2
2MgO+S、Mg+S
MgS)
| ||
| ||
| ||
(3)你认为该装置是否有不足之处?
有
有
,如果有,请列出两点:在A和B之间未连接一干燥装置;C装置未与大气相通;在镁下方未垫一不锈钢片,镁能与玻璃管反应;未设计防倒吸装置(任写两点即可)
在A和B之间未连接一干燥装置;C装置未与大气相通;在镁下方未垫一不锈钢片,镁能与玻璃管反应;未设计防倒吸装置(任写两点即可)
.