摘要:56%化学反应方程式书写11选择
网址:http://m.1010jiajiao.com/timu_id_127359[举报]
(2013?绵阳模拟)在某锂离子电池中,有一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如图1:
用相对分子质量为56的单烯烃A合成M的 方法可设计如图2:
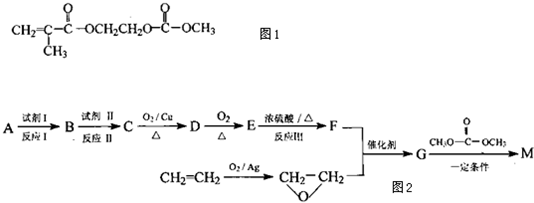
请回答下列问题:
(1)A的结构简式是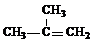
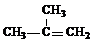 试剂Ⅱ是
试剂Ⅱ是
(2)G在一定条件下反应生成的高聚物是制备隐形眼镜的材料,请写出生成该高聚物的 化学反应方程式
(3)M与足量氯氧化钠溶液反应的化学方程式是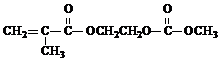 +3NaOH→
+3NaOH→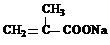 +HOCH2CH2OH+Na2CO3+CH3OH
+HOCH2CH2OH+Na2CO3+CH3OH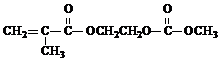 +3NaOH→
+3NaOH→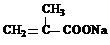 +HOCH2CH2OH+Na2CO3+CH3OH
+HOCH2CH2OH+Na2CO3+CH3OH
(4)在用E制备F的过程中,2分子的E反应会生成一种副产物,其核磁共振氢谱只有 一种吸收峰,该副产物的结构简式为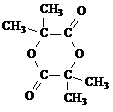
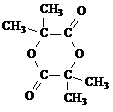 .
.
查看习题详情和答案>>
用相对分子质量为56的单烯烃A合成M的 方法可设计如图2:

请回答下列问题:
(1)A的结构简式是
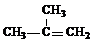
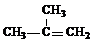
NaOH水溶液
NaOH水溶液
,反应Ⅲ的化学反应类型是消去反应
消去反应
.(2)G在一定条件下反应生成的高聚物是制备隐形眼镜的材料,请写出生成该高聚物的 化学反应方程式
n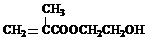
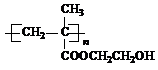
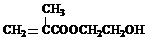
| 一定条件 |
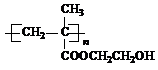
n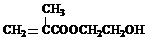
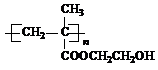
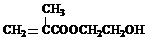
| 一定条件 |
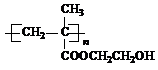
(3)M与足量氯氧化钠溶液反应的化学方程式是
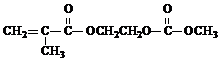 +3NaOH→
+3NaOH→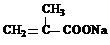 +HOCH2CH2OH+Na2CO3+CH3OH
+HOCH2CH2OH+Na2CO3+CH3OH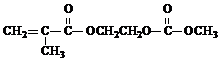 +3NaOH→
+3NaOH→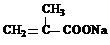 +HOCH2CH2OH+Na2CO3+CH3OH
+HOCH2CH2OH+Na2CO3+CH3OH(4)在用E制备F的过程中,2分子的E反应会生成一种副产物,其核磁共振氢谱只有 一种吸收峰,该副产物的结构简式为
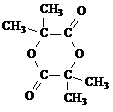
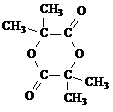
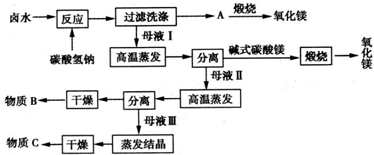
氧化镁主要用于制备陶瓷和耐火材料,医药上可用作抗酸剂.以卤水(主要含Mg2+Na+、Cl-、S
)为原料制取高纯氧化镁的工艺流程如图所示:
(1)反应温度对产品质量的影响情况如表所示:
由此可知,煅烧A生成MgO最适宜的温度为
(2)的主要成分是
(3)物质B和C的主要成分分别是
(4)写出碱式碳酸镁高温分解生成MgO的化学反应方程式:
查看习题详情和答案>>
| O | 2- 4 |

(1)反应温度对产品质量的影响情况如表所示:
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| MgO的质量分数/% | 97.75 | 97.56 | 97.86 | 99.13 | 99.01 |
60℃
60℃
,原因是该温度下产品中氧化镁质量分数相对较高
该温度下产品中氧化镁质量分数相对较高
(2)的主要成分是
MgCO3
MgCO3
(填化学式),确定A已洗涤干净的操作和现象是取最后一次的洗涤液,加入少量盐酸酸化的氯化钡溶液,若无沉淀产生,证明已经洗涤干净
取最后一次的洗涤液,加入少量盐酸酸化的氯化钡溶液,若无沉淀产生,证明已经洗涤干净
(3)物质B和C的主要成分分别是
硫酸钠、氯化钠
硫酸钠、氯化钠
(两者均写名称).(4)写出碱式碳酸镁高温分解生成MgO的化学反应方程式:
Mg2(OH)2CO3
2MgO+CO2↑+H2O↑
| ||
Mg2(OH)2CO3
2MgO+CO2↑+H2O↑
.
| ||
(2010?揭阳一模)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验可能用到的仪器如图所示:

[提出猜想]
Ⅰ.所得气体的成分可能只含
Ⅱ.所得气体的成分可能含有
Ⅲ.所得气体的成分可能含有
[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
(2)若实验结束,B中量筒没有收集到水,则证明猜想
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由.答:
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:
二组:
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是
查看习题详情和答案>>

[提出猜想]
Ⅰ.所得气体的成分可能只含
SO3
SO3
一种;Ⅱ.所得气体的成分可能含有
SO2、O2
SO2、O2
二种;Ⅲ.所得气体的成分可能含有
SO3、SO2、O2
SO3、SO2、O2
三种.[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
①⑨⑩⑥⑤③④⑧⑦②
①⑨⑩⑥⑤③④⑧⑦②
(填序号)(2)若实验结束,B中量筒没有收集到水,则证明猜想
Ⅰ
Ⅰ
正确.(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由.答:
不能,因为SO3与F中的饱和NaHSO3反应会生成等物质的量的SO2
不能,因为SO3与F中的饱和NaHSO3反应会生成等物质的量的SO2
.(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4 的质量(g) |
装置C增加 的质量(g) |
量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
一组:
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
| ||
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
;
| ||
二组:
2CuSO4
2CuO+2SO2↑+O2↑
| ||
2CuSO4
2CuO+2SO2↑+O2↑
.
| ||
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是
B
B
和E
E
(填代号).二甲基亚砜有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜( ),有关反应如下:
),有关反应如下:
反应①2CH3OH(l)+H2S(g)=(CH3)2S(l)+2H2O(l)△H=-akJ?mol-1
反应②(CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g)△H=-bkJ??mol-1
反应③2NO(g)+O2(g)=2NO2(g)△H=-ckJ?mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
(2)能说明反应2CH3OH(l)+H2S(g)?(CH3)2S(l)+2H2O(l)达平衡状态的是
A.v(CH3OH)=2v(H2S)
B.恒容容器中,体系的压强不再改变
C.恒容容器中,体系中气体的密度不再改变
D.恒容容器中,气体的摩尔质量不再改变
(3)反应③在一定条件下可达到平衡,则此条件下该反应平衡常数表达式K=
.

(4)上图是反应③在一定条件下发生反应,反应物和生成物能量与活化能的关系.在图中曲线
(5)N2O5是一种新型绿色硝化剂,其制备方法有以下两种.
方法一:4NO2(g)+O2(g)=2N2O5(g);△H=-56.76KJ?mol-1
常温下,该反应能逆向自发进行,则逆向反应的△S
方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:

硼氢化钠燃料电池的正极反应式
查看习题详情和答案>>
 ),有关反应如下:
),有关反应如下:反应①2CH3OH(l)+H2S(g)=(CH3)2S(l)+2H2O(l)△H=-akJ?mol-1
反应②(CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g)△H=-bkJ??mol-1
反应③2NO(g)+O2(g)=2NO2(g)△H=-ckJ?mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
2(CH3)2S(l)+O2(g)=2(CH3)2SO(l)△H=-(2b+c)kJ?mol-1
2(CH3)2S(l)+O2(g)=2(CH3)2SO(l)△H=-(2b+c)kJ?mol-1
,(2)能说明反应2CH3OH(l)+H2S(g)?(CH3)2S(l)+2H2O(l)达平衡状态的是
BC
BC
.A.v(CH3OH)=2v(H2S)
B.恒容容器中,体系的压强不再改变
C.恒容容器中,体系中气体的密度不再改变
D.恒容容器中,气体的摩尔质量不再改变
(3)反应③在一定条件下可达到平衡,则此条件下该反应平衡常数表达式K=
| c2(NO2) |
| C2(NO)c(O2) |
| c2(NO2) |
| C2(NO)c(O2) |

(4)上图是反应③在一定条件下发生反应,反应物和生成物能量与活化能的关系.在图中曲线
b
b
(填“a”或“b”)表示加入催化剂的能量变化曲线,催化剂能加快反应速率的原理是催化剂能降低该反应的活化能,提高活化分子的百分数,化学反应速率加快
催化剂能降低该反应的活化能,提高活化分子的百分数,化学反应速率加快
;(5)N2O5是一种新型绿色硝化剂,其制备方法有以下两种.
方法一:4NO2(g)+O2(g)=2N2O5(g);△H=-56.76KJ?mol-1
常温下,该反应能逆向自发进行,则逆向反应的△S
>
>
0(填“>、<”或“=”)方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5.工作原理如图:

硼氢化钠燃料电池的正极反应式
H2O2+2e-=2OH-
H2O2+2e-=2OH-
.(2011?濮阳二模)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如下图所示:

[提出假设]
Ⅰ.所得气体的成分可能只含
Ⅱ.所得气体的成分可能含有
Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种.
[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为
(2)实验过程中,仪器C的作用是
[验证假设,分析推理]
(3)若实验结束,B中量筒没有收集到水,则证明猜想
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同.数据如下:
请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式:
①组
查看习题详情和答案>>

[提出假设]
Ⅰ.所得气体的成分可能只含
SO3
SO3
一种;Ⅱ.所得气体的成分可能含有
SO2、O2
SO2、O2
二种;Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种.
[实验探究]
实验操作过程(略).已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为
①③④⑥⑤②
①③④⑥⑤②
(填序号).(2)实验过程中,仪器C的作用是
吸收SO2、SO3气体
吸收SO2、SO3气体
.[验证假设,分析推理]
(3)若实验结束,B中量筒没有收集到水,则证明猜想
I
I
正确.(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同.数据如下:
| 实验 小组 |
称取CuSO4 的质量/g |
仪器C增 加的质量/g |
量筒中水的体积折算成标 准状况下气体的体积/mL |
| ① | 6.4 | 2.88 | 224 |
| ② | 6.4 | 2.56 | 448 |
①组
4CuSO4
4CuO+2SO3↑+2SO2↑+O2↑
| ||
4CuSO4
4CuO+2SO3↑+2SO2↑+O2↑
;②组
| ||
2CuSO4
2CuO+2SO2↑+O2↑
| ||
2CuSO4
2CuO+2SO2↑+O2↑
.
| ||