0 42393 42401 42407 42411 42417 42419 42423 42429 42431 42437 42443 42447 42449 42453 42459 42461 42467 42471 42473 42477 42479 42483 42485 42487 42488 42489 42491 42492 42493 42495 42497 42501 42503 42507 42509 42513 42519 42521 42527 42531 42533 42537 42543 42549 42551 42557 42561 42563 42569 42573 42579 42587 447348
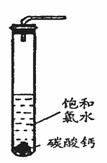
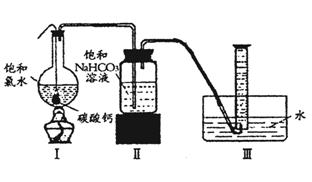 在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。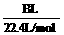 明显小于
明显小于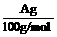 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
 ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;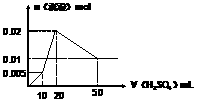
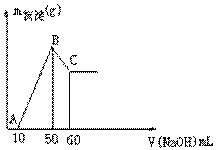 (12分)把一小块镁铝合金溶于100mL盐酸中,
(12分)把一小块镁铝合金溶于100mL盐酸中,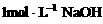 溶液,生成沉淀
溶液,生成沉淀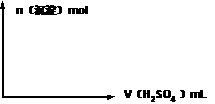 (5)若将此小块镁铝合金先加入10mL 1mol/LBa(OH)2
(5)若将此小块镁铝合金先加入10mL 1mol/LBa(OH)2