21.已知某化学反应的平衡常数表达式为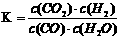 ,在不同的温度下该反应的平衡常数如下表:
,在不同的温度下该反应的平衡常数如下表:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
1.67 |
1.11 |
1.00 |
0.60 |
0.38 |
下列有关叙述不正确的是
A.该反应的化学方程式是CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.若在一定体积的密闭容器中通入CO2和H2各1mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态
D.若平衡浓度符合下列关系式: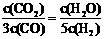 ,则此时的温度为1000℃
,则此时的温度为1000℃
18.熵变、焓变可作为反应过程进行方向的判据,下列反应一定有自发倾向的是
A.△H < 0 △S > 0 B.△H > 0 △S < 0
C.△H < 0 △S < 0 D.△H > 0 △S > 0
16.下表为部分短周期元素的原子半径及其主要化合价,
|
元素代号 |
L |
M |
R |
T |
|
原子半径 / nm |
0.160 |
0.143 |
0.104 |
0.066 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
-2 |
根据表中信息,判断下列叙述正确的是
A.L2+与R2-有相同的电子层结构 B.氢化物的形成难易及稳定性H2T<H2R
C.M2T3具有两性 D.单质与 稀硫酸反应的速率为L<M
稀硫酸反应的速率为L<M
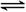 n C(g),1 min时达到平衡,C的浓度为x mol/L。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8x mol/L。 下列说法正确的是
n C(g),1 min时达到平衡,C的浓度为x mol/L。若保持温度不变,将密闭容器的容积压缩为原来的1/2,达到新的平衡时C的浓度为1.8x mol/L。 下列说法正确的是