28.(10分)X、Y、Z、Q、E五种元素中,X原子核外的M层中有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在
水中的溶解度较大的是 (写分子式),
(3)Q的元素符号是 ,它属于第 周期,它的外围外电子排布式
为 _________________,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键___________________________________________________________________
29(15分)下表列出前20号元素中的某些元素性质的一些数据:
|
元素 性质 |
A |
B |
C |
D |
E |
F |
G |
H |
I |
J |
|
原子半径(10-10m) |
1.02 |
2.27 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.86 |
0.75 |
1.17 |
|
最高价态 |
+6 |
+1 |
- |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
+4 |
|
最低价态 |
-2 |
- |
-2 |
- |
-4 |
-3 |
-1 |
- |
-3 |
-4 |
试回答下列问题:
(1)以上10种元素中第一电离能最小的是: (填编号)。
(2) 写出下列有关反应的化学方程式:
① E的单质与I元素的最高价氧化物对应的水化物浓溶液反应:
__________________________________________________________________;
② H2C2与EC2反应:
__________________________________________________________________。
(3)上述E、F、G三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的是 __ (写分子式只写2种)。元素I形成的单质分子中含有_ ______个π键。比元素B原子序数大10的元素基态原子外围电子排布式 。
(4)H--C≡C-CHBr-CH3分子中碳元素原子以 __ 和 __ 杂化成键,分子中共形成 _________个σ键, __________个π键, 是否是手性分子___________
(5)E和I相比较,非金属性强弱,可以验证你的结论的是下列中的 (填编号)。
a.气态氢化物的稳定性 b. 单质分子中的键能
c. 两元素的电负性 d .最高价含氧酸的酸性
辽宁鞍山市第十三中学09-10学年度高二下学期
27.按要求填写(6分)
|
化学式 |
中心原子孤电子对数 |
杂化轨道数 |
杂化轨道类型 |
分子空间构型 |
|
CO2 |
|
|
|
|
|
SO2 |
|
|
|
|
|
BF3 |
|
|
|
|
|
H3O+ |
|
|
|
|
|
CHCl3 |
|
|
|
|
|
SCl2 |
|
|
|
|
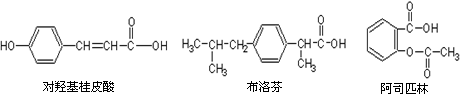 下列三种有机物是某些药物中的有效成分:
下列三种有机物是某些药物中的有效成分: 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 ③⑤⑥⑧ D.⑤⑥⑦⑧
③⑤⑥⑧ D.⑤⑥⑦⑧