16.某实验兴趣小组对NaHCO3饱和溶液的pH随温度的变化进行了测量,实验数据记录如下:(改编)
|
温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
(1)甲同学认为,NaHCO3饱和溶液pH升高的原因有两种可能:
①一是HCO3-的水解程度随温度升高而增大,故碱性增强,离子方程式为 ;
②二是 ;
(2)请你设计一个简单的实验以确定NaHCO3饱和溶液的pH随温度升高的原因,简述实验方法和结论:
答案:(1)①HCO3-+H2O H2CO3+OH-;
H2CO3+OH-;
②NaHCO3受热分解生成了更易水解的Na2CO3
(2)向加热煮沸的NaHCO3溶液中加入足量的BaCl2溶液,若产生白色沉淀,则是原因②;否则为原因①或者将加热后的溶液冷却到10℃,若溶液的pH=8.3,则为原因①;若溶液的pH>8.3,则为原因②。

 B.
B.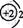 C.
C. D.
D.
 N2O4)。(改编)
N2O4)。(改编) (1) 0.004molCu被硝酸完全溶解后,Cu失去的电子数是______________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为____________。
(1) 0.004molCu被硝酸完全溶解后,Cu失去的电子数是______________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为____________。 =
3Cu2++NO↑+3NO2↑+5H2O
=
3Cu2++NO↑+3NO2↑+5H2O 甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如下图所示的转化关系。(原创)
甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如下图所示的转化关系。(原创) 2MgO+S、2Mg+SiO2
2MgO+S、2Mg+SiO2
 ②CH2==CH-CH==CH2+Br2
CH2Br-CH==CH-CH2Br
②CH2==CH-CH==CH2+Br2
CH2Br-CH==CH-CH2Br

 答案:(1)
答案:(1)

 (2)①水解反应(取代反应);加成反应;
(2)①水解反应(取代反应);加成反应;
 ③
③ BrCH2-C(CH3)==CH-CH2Br+2NaOH
BrCH2-C(CH3)==CH-CH2Br+2NaOH

 某研究性学习小组为验证在相同条件下,相同浓度的一元强酸和一元弱酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如下图所示的简易实验装置。该实验的主要操作步骤如下:(改编)
某研究性学习小组为验证在相同条件下,相同浓度的一元强酸和一元弱酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如下图所示的简易实验装置。该实验的主要操作步骤如下:(改编)
