22.有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化。
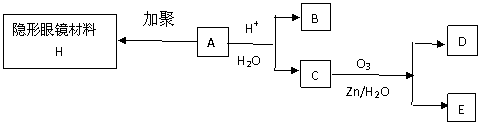
已知:(1)物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。常温下E为气体。




|




|
 = =O
+ O=
= =O
+ O=
R3 H H
R3
回答下列问题:
(1)A中不含氧官能团的名称 ;E的水溶液的一种用途 ;
(2)写出物质B在铜的催化下与氧气反应的化学方程式
;
(3)C与氢气加成产物F的同分异构体中,分子为链状的酯类物质共有 种,
其中能够发生银镜反应的酯的结构简式 ;
(4)隐形眼镜材料H的结构简式为 ,H作为隐形眼镜的材料,具有良好的透气性和亲水性,请从H的结构分析,他可以作为隐形眼镜材料的原因是
;
(5)请设计合理的方案,用物质D制取乙二酸。


 H2C=CH-COOH
H2C=CH-COOH
|
|
||||||
|
|||||||

|

|
中间产物
高二第一学期期末教学质量检测
19.(10分)将下列表中括号内的物质为所含的少量杂质,请选用最佳的试剂和分离装置将杂质除去,将对应的编号填入表中。试剂: a水,b饱和碳酸钠溶液,c 溴水,d 酸性高锰酸钾溶液,e生石灰, f NaOH溶液分离装置:A分液装置,B过滤装置,C蒸馏装置,D洗气装置。
|
|
需加入的试剂 |
分 离 装 置 |
|
CH3CH2OH(水) |
|
|
|
乙烷(乙烯) |
|
|
|
苯(甲苯) |
|
|
|
苯(苯酚) |
|
|
|
乙酸乙酯(乙酸和乙醇) |
|
|
20(8分)已知1 molCO气体完全燃烧生成CO2 气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气燃烧的热化学反应方程式 。
(2)若1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量为 890 kJ( 填“>”、 “<”、“= ”)。若甲醇的燃烧热为726.0 kJ·mol-1,试根据盖斯定律计算并写出甲烷催化氧化生成甲醇的热化学方程式
。
(3)若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的取值范围是 。
21(10分)火法炼锌就是将闪锌矿(主要含ZnS)通过浮选、焙烧使之转化为氧化锌,再把氧化锌与足量焦炭混合,在鼓风炉中加热至1100℃至1300℃,将锌蒸馏出来。涉及的主要反应为:焙烧炉中:2ZnS + 3 O2=2ZnO+2SO2 ①;
鼓风炉中:2C + O2 = 2CO ②;ZnO(s)
+ CO(g)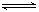 Zn(g) + CO2(g) ③.假设鼓风炉体积固定且密闭,随着反应进行,鼓风炉内气体物质的量浓度随时间的变化关系如下表:
Zn(g) + CO2(g) ③.假设鼓风炉体积固定且密闭,随着反应进行,鼓风炉内气体物质的量浓度随时间的变化关系如下表:
|
反应进行时间/min |
c(CO) / mol/L |
c(Zn)/ mol/L |
c(CO2)/ mol/L |
|
0 |
0.11 |
0 |
0 |
|
2 |
0.1 |
0.01 |
0.01 |
|
30 |
c1 |
c2 |
c2 |
|
35 |
c1 |
c2 |
c2 |
请回答下列问题:
(1)若保持温度不变,在鼓风炉中增大CO的浓度,反应③的平衡常数K值
(填“增大”、“减小”或“不变”)
(2)已知该温度时,反应③的化学平衡常数K=1.0,则上表中c1= .
( 3 )假设通过改变反应条件,使在焙烧炉中生成的ZnO几乎完全被CO还原,则焙烧炉与鼓风炉中消耗O2的体积不超过 。
(4)若起始浓度不变,通过改变反应条件,达平衡时鼓风炉中反应③CO的转化率为80%,此时该反应的平衡常数K= ;此时焙烧炉和鼓风炉中消耗O2的体积比应大于 .
 B.CCl4的电子式:
B.CCl4的电子式: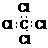
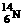 D.邻甲苯酚的结构简式:
D.邻甲苯酚的结构简式: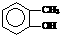
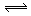 2H++C2O
2H++C2O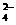
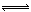 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是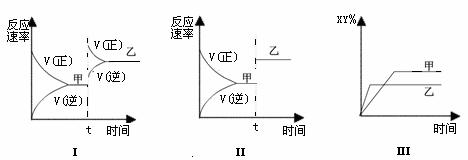

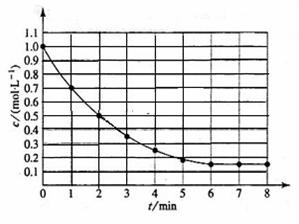 下图表示反应X(g) 4Y(g)+Z(g)
下图表示反应X(g) 4Y(g)+Z(g) 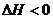 ,在某温度时X的浓度随时间变化的曲线:
,在某温度时X的浓度随时间变化的曲线: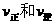 将以同样倍数减小
将以同样倍数减小