11(15分)浓H2SO4和木炭在加热时发生反应的化学方程式是
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
 请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
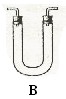
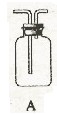
将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
|
|
12(16分)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:

(1)溶解大理石时,用硝酸而不同硫酸的原因是_______________________________;
(2)操作Ⅱ的目的是______________,溶液A(溶质是共价化合物)是___________;
(3)写出检验滤液中是否含铁离子方程式:_____________________________________
______________________________________________________________________;
(4)写出加入碳酸铵所发生反应的离子方程式:________________________________;
写出滤液B的一种用途:_________________________;
(5)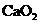 中一般含
中一般含 。试按下列提示完成
。试按下列提示完成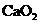 含量分析的实验设计。
含量分析的实验设计。
试剂:氢氧化钠标准溶液、盐酸标准溶液、酚酞 仪器:电子天平、锥形瓶、滴定管
实验步骤:
① ;②加入 ;③加入酚酞,用氢氧化钠标准溶液滴定。
13(19分)某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将 氧化成
氧化成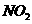 ,而稀硝酸不能氧化
,而稀硝酸不能氧化 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与 反应,能与
反应,能与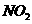 反应
反应

(1)实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
;
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
;
(3)装置①中发生反应的化学方程式是 ;
(4)装置②的作用是 ,发生反应的化学方程式是 ;
(5)该小组得出的结论的试验现象是
;
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母) 。
a. 加热该绿色溶液,观察颜色变化
b. 加水稀释绿色溶液,观察颜色变化
c. 向该绿色溶液中通入氮气,观察颜色变化
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
广东省增城中学2010届高三化学晚练
 ,若要使溴水的颜色变浅,可采取的措施是
,若要使溴水的颜色变浅,可采取的措施是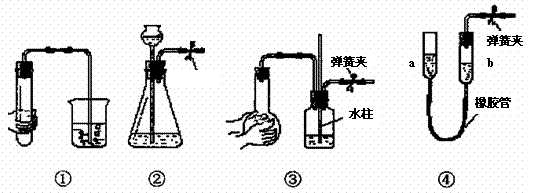 A.对装置①,双手移去后.导管中水面与烧杯水面相平
A.对装置①,双手移去后.导管中水面与烧杯水面相平