25.同学们都有这样的学习、生活经验:木炭在氧气中燃烧比空气中燃烧得更旺;夏天,将食品放在冰箱里不容易腐烂。说明反应物的浓度和温度对化学反应快慢(反应速率)有影响。那么,浓度和温度是如何影响化学反应速率的?
(1)提出假设:a.浓度越大,化学反应越快;b.温度越高,化学反应越快。
(2)设计方案:同学们利用铁粉和盐酸反应来探究上述问题,设计了下列3组实验。
|
组别 |
温度/℃ |
铁粉质量/g |
盐酸的质量分数和体积 |
观察气泡产生的速率 |
|
1 |
10 |
2.8 |
10%、50 mL |
|
|
2 |
10 |
2.8 |
20%、50 mL |
|
|
3 |
20 |
2.8 |
10%、50 mL |
|
(3)分析探究:将铁粉加入到盛盐酸的烧杯中发生反应,写出反应的化学方程式__________________。哪两组实验用来探究“温度越高,化学反应越快”的假设? ___ 。
(4)讨论反思:事实上,化学反应的发生,是反应物的微观粒子相互接触、碰撞的结果。请你解释“盐酸浓度越大,与铁粉反应越快”的原因 _______________ ____。
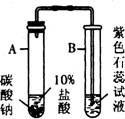
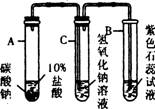
 次氯酸钙中氯元素的化合价是________。
次氯酸钙中氯元素的化合价是________。
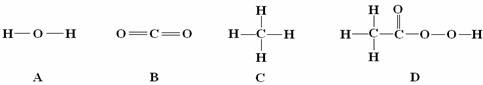
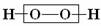 “物质的结构决定性质,物质的性质决定用途”是科学的重要思想。过氧化氢是一种常用的杀菌消毒剂,其原因是过氧化氢分子中含有一种叫“过氧基”的结构(如图中方框框出部分)。据此推测下列物质中,也可作杀菌消毒剂的是----------------------------------------------------------------------------( )
“物质的结构决定性质,物质的性质决定用途”是科学的重要思想。过氧化氢是一种常用的杀菌消毒剂,其原因是过氧化氢分子中含有一种叫“过氧基”的结构(如图中方框框出部分)。据此推测下列物质中,也可作杀菌消毒剂的是----------------------------------------------------------------------------( )