0 38419 38427 38433 38437 38443 38445 38449 38455 38457 38463 38469 38473 38475 38479 38485 38487 38493 38497 38499 38503 38505 38509 38511 38513 38514 38515 38517 38518 38519 38521 38523 38527 38529 38533 38535 38539 38545 38547 38553 38557 38559 38563 38569 38575 38577 38583 38587 38589 38595 38599 38605 38613 447348
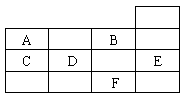 右表为元素周期表前四周期的一部分,下列有关A、B、C、D、E、F六种元素的叙述正确的是 ( )
右表为元素周期表前四周期的一部分,下列有关A、B、C、D、E、F六种元素的叙述正确的是 ( )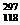 X),它的存在时间仅为0.9毫秒,然后首先释放出一颗由两个质子和两个中子组成的α粒子,衰变为已知的116号元素,然后再度释放出一颗α粒子,衰变为114号元素。按照元素周期表排序规律及原子结构知识,有关这个新的118号元素的说法肯定不正确的是
( )
X),它的存在时间仅为0.9毫秒,然后首先释放出一颗由两个质子和两个中子组成的α粒子,衰变为已知的116号元素,然后再度释放出一颗α粒子,衰变为114号元素。按照元素周期表排序规律及原子结构知识,有关这个新的118号元素的说法肯定不正确的是
( )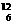 C相对原子质量之比为118∶6
C相对原子质量之比为118∶6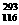 Y
Y 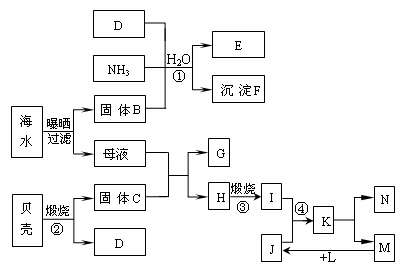 试填写下列空白:
试填写下列空白: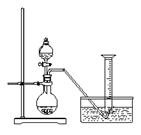 9 (11分) 某同学设计了如下方案,来测定过氧化钠样品的纯度(杂质不参加反应,条件为标准状况)。
9 (11分) 某同学设计了如下方案,来测定过氧化钠样品的纯度(杂质不参加反应,条件为标准状况)。 白色沉淀
白色沉淀 放出使湿润的红色石蕊试纸变蓝的气体
放出使湿润的红色石蕊试纸变蓝的气体