17. 某实验小组测定某常用食醋的酸量(g/L),拟采用以下方法:
⑴甲同学粗测食醋的酸度:用pH试纸测溶液pH的方法是
。
⑵乙同学较精确的测定食醋的pH:所用仪器是 。
⑶丙同学由乙同学所测结果(pH=2.00)计算得该常用食醋的酸量为0.6 g/L,明显低于正常含量(30~50g/L)其原因是:
⑷丁同学认为以上方法均不能准确测定食醋的酸量并提出中和测定法。甲同学用pH试纸 (填能、否)粗略测得食醋的酸度;要在滴定时准确判断滴定终点,还必须对食醋作何处理?
(5)该实验小组欲测定某市售食用白醋的总酸量(单位:g/100mL),设计实验如下:
Ⅰ.试剂和用品
白醋样品100mL、0.1000 mol·L-1 NaOH标准溶液、蒸馏水、0.1%甲基橙溶液、0.1%酚酞溶液、0.1%石蕊溶液
100 mL容量瓶、玻璃棒、胶头滴管、50 mL酸式滴定管、50 mL碱式滴定管、滴定管夹、铁架台、100 mL烧杯、酒精灯、火柴、三脚架、石棉网、pH计
Ⅱ.实验步骤
①用50 mL酸式滴定管移取10mL市售白醋样品,置于100mL容量瓶中,加蒸馏水(煮沸除去CO2并迅速冷却)稀释至刻度线,摇匀即得待测食醋溶液。
②用酸式滴定管量取待测白醋溶液20.00 mL。
③盛装标准NaOH溶液,静置后,读取数据,记录为NaOH标准溶液体积的初读数。
④滴定,并记录NaOH的终读数。重复滴定2-3次,数据记录如下。
|
滴定次数 实验数据 |
1 |
2 |
3 |
4 |
|
V(样品)/mL |
20.00 |
20.00 |
20.00 |
20.00 |
|
V(NaOH)/mL(初读数) |
0.10 |
0.30 |
0.00 |
0.20 |
|
V(NaOH)/mL(终读数) |
20.08 |
20.30 |
20.80 |
20.22 |
|
V(NaOH)/mL(消耗) |
19.98 |
20.00 |
20.80 |
20.02 |
Ⅲ.数据处理与问题讨论
①本实验需要的试剂是 ,还缺少的一种仪器是________________。
②滴定过程中使用pH计将溶液的pH变化情况记录如下表。
|
V(NaOH)/mL |
0.00 |
10.00 |
18.00 |
19.80 |
19.98 |
20.00 |
20.02 |
20.20 |
22.00 |
|
溶液pH |
2.88 |
4.70 |
5.70 |
6.74 |
7.74 |
8.72 |
9.70 |
10.70 |
11.70 |
在允许的误差范围(±0.1%)内,pH突变的范围为______,所以可选择_______作指示剂。
③甲同学在处理数据过程中计算得到平均消耗的NaOH溶液的体积为:
V(NaOH)=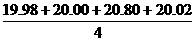 =20.20 mL
=20.20 mL
他的计算合理吗?理由是________________________________________________。
④该市售白醋样品中醋酸的物质的量浓度是_____________mol·L-1,样品总酸量为___________g/100mL。
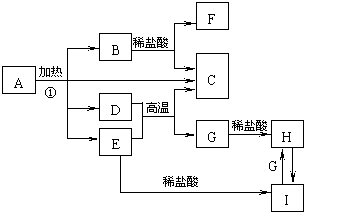 化合物A是一种重要的光化学试剂,属不含结晶水的复盐。A-H之间相互转化关系如下图所示:(部分反应物、生成物没有列出)
化合物A是一种重要的光化学试剂,属不含结晶水的复盐。A-H之间相互转化关系如下图所示:(部分反应物、生成物没有列出)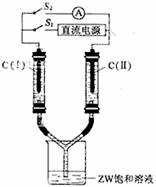 (3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
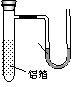 (C)铝与氧气反应放出大量的热量
(D)铝片上生成的白毛是氧化铝和氧化汞的混合物
(C)铝与氧气反应放出大量的热量
(D)铝片上生成的白毛是氧化铝和氧化汞的混合物
 2C(g)+D(g);△H<0。现将1mol
A和2molB加入甲容器中,将4 molC和2
mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g);△H<0。现将1mol
A和2molB加入甲容器中,将4 molC和2
mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )