0 38367 38375 38381 38385 38391 38393 38397 38403 38405 38411 38417 38421 38423 38427 38433 38435 38441 38445 38447 38451 38453 38457 38459 38461 38462 38463 38465 38466 38467 38469 38471 38475 38477 38481 38483 38487 38493 38495 38501 38505 38507 38511 38517 38523 38525 38531 38535 38537 38543 38547 38553 38561 447348
 2HI(g);△H>O,当达到平衡后,t0时改变反应的某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是
2HI(g);△H>O,当达到平衡后,t0时改变反应的某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是
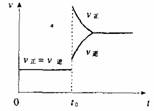 A.容器内气体颜色变深,平均分子量不变
A.容器内气体颜色变深,平均分子量不变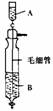 A.A中装浓硫酸,B中装浓盐酸
A.A中装浓硫酸,B中装浓盐酸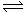 XeF2;XeF2+F2
XeF2;XeF2+F2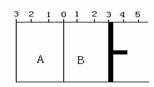 (1)温度升高,平衡移动后达到新的平衡,高炉内CO2和CO的体积比值 (填“增大”“减小”或“不变”),平衡常数k值 (填“增大”“减小”或“不变”)。
(1)温度升高,平衡移动后达到新的平衡,高炉内CO2和CO的体积比值 (填“增大”“减小”或“不变”),平衡常数k值 (填“增大”“减小”或“不变”)。 2 SO3(g)。根据下列要求填写空白:
2 SO3(g)。根据下列要求填写空白: