已知:⑴ 凡与醛基直接相连的碳原子上的氢称为α一H原子,在稀碱溶液的催化作用下,一个醛分子上的α一H原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:
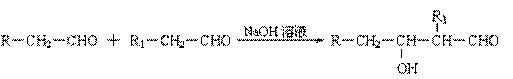
 ⑵
⑵
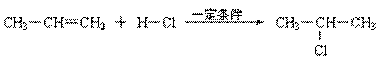
⑶合成路线如下:
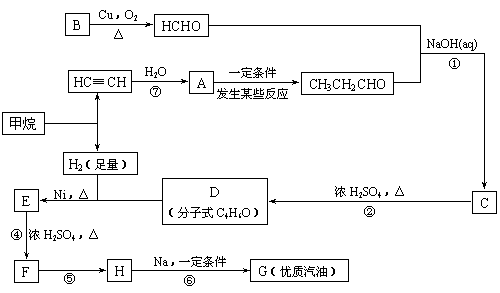
(1)写出D的结构简式
(2)在反应②-⑦中,属于加成反应的是 ,属于消去反应的是 。
(3)写出反应方程式
E → F: ;
(4)H也能与NaOH水溶液反应,其反应方程式为
。
28(B)(10分)下表是元素周期表中第一、第二周期10种元素的某种性质的一组数据(所列数据的单位是相同的)。除带“……”的四种元素除外,其余元素都给出了该种元素的全部该类数据。
|
(H) 13.6 |
|
|
|
|
|
|
(He) 24.6 54.4 |
|
(Li) 5.4 75.6 122.5 |
(Be) 9.3 18.2 153.9 217.7 |
(B) 8.3 25.2 37.9 259.4 340.2 |
(C) 11.3 24.4 47.9 64.5 392.1 489.9 |
(N) 14.5 29.6 47.4 72.5 97.9 552.1 …… |
(O) 13.6 35.1 …… …… …… …… …… …… |
(F) 17.4 34.9 …… …… …… …… …… …… …… |
(Ne) 21.6 41.6 …… …… …… …… …… …… …… …… |
研究这些数据:
(1)每组数据可能是该元素的________________
A.原子得到电子所放出的能量 B.原子半径的大小
C.原子逐个失去电子所吸收的能量 D.原子及形成不同分子的半径的大小
(2)分析同周期自左往右各元素原子的第一个数据
①总体变化趋势是_______(填“增大”或“减小”),②与前后元素相比,由于该元素的数值增大得较多而变为反常的元素是在________族,分析它们的原子核外电子排布后,指出造成上述反常情况的可能原因是_________________
A.它们的原子半径突然变小些 B.它们的核外电子排布处于饱和状态
C.它们的原子半径突然变大些 D.它们的核外电子排布处于半充满或全充满状态
根据以上规律,请推测镁和铝的第一个数据的大小Mg(1)_____Al(1)
(3)同一元素原子的一组数据是约以倍比关系增大,请你说出可能的一个原因是_________________________________________________,每个元素的一组数据中个别地方增大的比例特别大,形成突跃(大幅度增大),请找出这些数据,并根据这些数据出现的规律,你认为氧元素出现该情况的数据应该是氧元素8个数据的第_______个。
上述规律可以证明原子结构中_______________________________的结论。
 下列化学用语表达正确的是
下列化学用语表达正确的是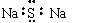 B.Na2S的电子式:
B.Na2S的电子式: 下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。 (14分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
(14分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得: (1)某校化学研究性学习小组的同学在技术人员的指导下,按下列
(1)某校化学研究性学习小组的同学在技术人员的指导下,按下列
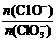 2(填“>”、“<”或“=”);
2(填“>”、“<”或“=”);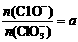 ,则n(C1-)= mol(用含a的代数式来表示)。
,则n(C1-)= mol(用含a的代数式来表示)。