25.(10分)我国规定饮用水质量标准必须符合下列要求:
|
PH值 |
6.5-8.5 |
|
Ca2+,Mg2+总浓度 |
< 0.0045mol/L |
|
细菌总数 |
< 100个/mL |
以下是源水处理成自来水的工艺流程示意图

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式____ _________
(2)凝聚剂除去悬浮固体颗粒的过程__________(填写编号,多选倒扣)
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O常用的凝聚剂,它在水中最终生成_____ ______沉淀。
(3)通入二氧化碳的目的是__________ _______和_______ ______。
(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有______________性,请写出氯气与水反应的离子反应方程式 。
(5)下列物质中能作为氯气的代用品的是 (填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
24.(10分)工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)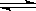 2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下:
2NH3(g),△H = -92.44kJ/mol;其部分工艺流程如下:
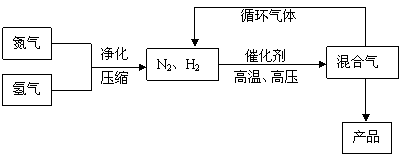
反应体系中各组分的部分性质见下表:
|
气体 |
氮气 |
氢气 |
氨 |
|
熔点(℃) |
-210.01 |
-252.77 |
-77.74 |
|
沸点(℃) |
-195.79 |
-259.23 |
-33.42 |
回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度的升高,K值 (填增大、减小、不变)。
(2)平衡常数K值越大,表明 (填序号)。
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。
 D. S2-的最外层电子排布式:3s23p4
D. S2-的最外层电子排布式:3s23p4 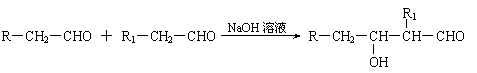 (1)凡与醛基直接相连的碳原子上的氢称为α-H原子,在稀碱溶液的催化作用下,一个醛分子上的α-H原子连接到另一个醛分子中醛基的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:
(1)凡与醛基直接相连的碳原子上的氢称为α-H原子,在稀碱溶液的催化作用下,一个醛分子上的α-H原子连接到另一个醛分子中醛基的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如: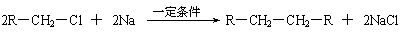 (2)
(2)
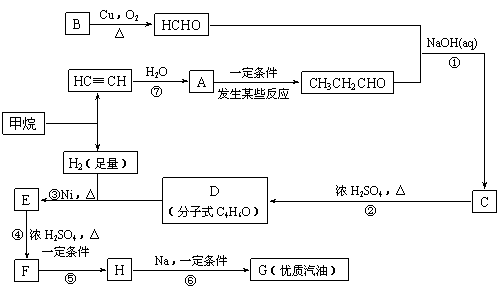
 (10分)新型节能材料高温超导体的最先突破是在1987年
(10分)新型节能材料高温超导体的最先突破是在1987年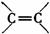 的化合物与CH2==CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2==CH2一样,在一定条件下可聚合成高分子化合物。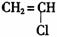 聚合而成的,其化学方程式是
聚合而成的,其化学方程式是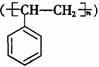 ,它是由 (写结构简式)聚合而成。
,它是由 (写结构简式)聚合而成。