0 37913 37921 37927 37931 37937 37939 37943 37949 37951 37957 37963 37967 37969 37973 37979 37981 37987 37991 37993 37997 37999 38003 38005 38007 38008 38009 38011 38012 38013 38015 38017 38021 38023 38027 38029 38033 38039 38041 38047 38051 38053 38057 38063 38069 38071 38077 38081 38083 38089 38093 38099 38107 447348





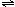 2NH3(g);△H=-Q1 kJ/mol(Q1>0)
2NH3(g);△H=-Q1 kJ/mol(Q1>0) D.HS-的水解:HS- + H2O
D.HS-的水解:HS- + H2O 利用维生素C能使淀粉-碘溶液褪色的性质,通过实验(如图所示)比较加入苹果汁和橙汁的多少来确定它们中维生素C含量的多少。要得出正确结论,在实验时需要控制的条件是
利用维生素C能使淀粉-碘溶液褪色的性质,通过实验(如图所示)比较加入苹果汁和橙汁的多少来确定它们中维生素C含量的多少。要得出正确结论,在实验时需要控制的条件是 A.原子半径大小比较为A>B>C>D
A.原子半径大小比较为A>B>C>D