22.(10分)某些废旧塑料可采用下列方法处理:将废塑料
隔绝空气加强热,使其变成有用的物质。
实验装置如右图:
加热聚丙烯废塑料得到的产物如下表:
|
产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
|
质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |
⑴ 试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
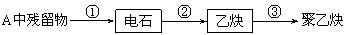
写出反应②、③的化学方程式______________________、______________________。
⑵ 试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有______种。
⑶ 锥形瓶C中观察到的现象______________________。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为_______________。
⑷ 写出C中逸出的气体在工业上的两种用途________________、__________________。
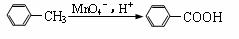

甲:将锌放入浓盐酸中,反应速率较快
乙:将实验过程记录下来,并交流。

根据上述资料与交流材料回答下列列问题
⑴乙反应速率明显比甲快,原因是: 。
⑵丙、丁根据铜位于金属活动顺序表氢之后,与盐酸不反应,对乙产生的气体体积比甲大的事实。作出如下推断:
①丙认为是溶解在溶液中的H2逸出,你认为是否有道理,理由是: ________。
②丁作了如下猜想,是否成立,请你设计实验方案。
|
丁猜想 |
验证方法 |
预测现象及结论 |
|
丁认为铜片中可能含有锌等杂质 |
|
|
⑶戊注意到乙中(3)中的白色沉淀,分析:不可能是CuCl2,因为CuCl2溶液显蓝色或绿色,也不可能是氯化锌,因为稀释后溶液更稀,不会析出。并利用资料①②大胆猜想,白色沉淀是生成的氯化亚铜。请你帮他设计验证方案(若有多个只设计一个方案):
|
戊 |
预计验证方法 |
预测的现象与结论 |
|
白色沉淀是氯化亚铜 |
|
⑷指导老师肯定了戊的猜想,请结合资料③,写出铜与足量浓盐酸在加热条件下反应生成无色溶液及气体,化学方程式可能是: 。
乙的实验步骤(3)稀释,生成沉淀,实际上是一个平衡问题,请写出这一平衡关系:
(用离子方程式表示)。
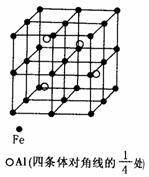 (1)确定该合金的化学式__________________;
(1)确定该合金的化学式__________________; 以下是用苯作原料制备一系列化合物的转化关系图:
以下是用苯作原料制备一系列化合物的转化关系图: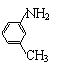 E________________________,F____________________________。
E________________________,F____________________________。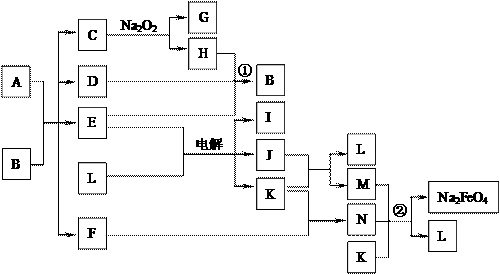
 ⑶甲和乙的化学式分别为 、
,若A中组成元素的物质的量之比为4∶9,则乙在A中的物质的量分数为
。
⑶甲和乙的化学式分别为 、
,若A中组成元素的物质的量之比为4∶9,则乙在A中的物质的量分数为
。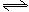 2SO3 (g) △H=-196.6kJ/mol
2SO3 (g) △H=-196.6kJ/mol

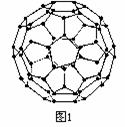 (8分)20世纪80年代日本科学家应用电子计算机模拟出结构类似于C60(分子结构如右图1所示)的物质N60,计算机模拟结果显示,N60与C60有相似的结构但稳定性较差。科学家预测,将N2进行冷冻或加压,然后运用高强度激光照射能转变为N60分子团,该分子团具有极强的挥发性,在受热情况下瞬间分解为N2并释放出大量的能量,2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮(局部结构如右图2),这种高聚氮的晶体中每个氮原子都通过三根单键与其它氮原子结合并向空间发展构成立体网状结构。
(8分)20世纪80年代日本科学家应用电子计算机模拟出结构类似于C60(分子结构如右图1所示)的物质N60,计算机模拟结果显示,N60与C60有相似的结构但稳定性较差。科学家预测,将N2进行冷冻或加压,然后运用高强度激光照射能转变为N60分子团,该分子团具有极强的挥发性,在受热情况下瞬间分解为N2并释放出大量的能量,2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮(局部结构如右图2),这种高聚氮的晶体中每个氮原子都通过三根单键与其它氮原子结合并向空间发展构成立体网状结构。