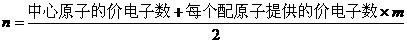
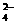21.(10分)分子(或离子)的空间构型有直线形、角形、平面形、四面体形、三角锥形等。为了解释和预测分子的空间构型,科学家在归纳了已知分子的空间构型的基础上,提出一种简单的理论模型,其理论依据是:分子中的价电子对(包括成键电子对和孤对电子)由于相互排斥作用,而取向彼此远离以减小斥力,分子尽可能采取对称的空间构型。对于ABm形分子(A为中心原子,B为配位原子),分子中的价电子对数(n)可以通过下式确定:
|
分子构型 |
AB2 |
AB3 |
AB2 |
AB3 |
AB4 |
|
价电子对数 |
2 |
3 |
4 |
4 |
4 |
|
几何构型 |
直线形 |
平面形 |
角形 |
三角锥形 |
四面体形 |
说明:①作为配位原子,氧原子、硫原子按不提供价电子计算;
②直线形分子中最少有3个原子,平面形分子中最少有4个原子。
(1)指出下面物质分子或离子的空间构型:
PO43- CS2 A1Br3
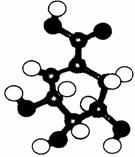
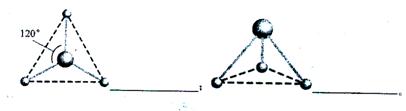 (2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
(3)按要求写出第二周期非金属元素构成中性分子的化学式:
平面形分子 ,三角锥形分子 ,四面体形分子 。
19.现有100mL溶质为MgC12和A1C13的混合溶液,其中c(C1-)=1.0mol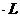
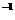 ,c(MG2+)=0.2mol
,c(MG2+)=0.2mol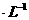 。若不考虑水解因素,则要使其中的Mg2+全部转化Mg(OH)2沉淀而分离出来,至少需要4mol
。若不考虑水解因素,则要使其中的Mg2+全部转化Mg(OH)2沉淀而分离出来,至少需要4mol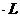 -1的NaOH溶液的体积是
-1的NaOH溶液的体积是
A.25mL B.5mL C.30mL D.100mL
姓名 学号
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
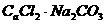 B.
B.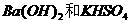
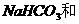 HCl D.
HCl D.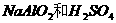
 请回答下列问题:
请回答下列问题: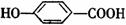 ,该反应的化学方程式是 。
,该反应的化学方程式是 。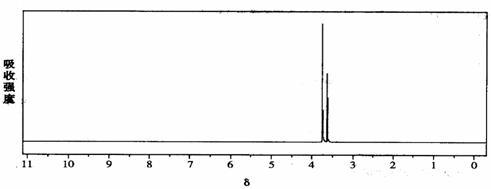
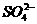 还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。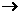 CH3CH3+2CO2
CH3CH3+2CO2 +H2
+H2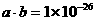 ,该溶液中可能大量共存的离子是
,该溶液中可能大量共存的离子是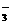 ②Na+、NO
②Na+、NO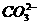
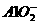 ④
④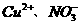 、A13+、SO
、A13+、SO