19、有A、B、C、D、E、F六种元素,已知 :它们位于三个不同短周期,核电荷数依次增大:A与E、B与F分别同主族;A、E分别都能与D按原子个数比1∶1或2∶l形成化合物;B、C分别都能与D按原子个数比1∶1或1∶2形成化合物。
:它们位于三个不同短周期,核电荷数依次增大:A与E、B与F分别同主族;A、E分别都能与D按原子个数比1∶1或2∶l形成化合物;B、C分别都能与D按原子个数比1∶1或1∶2形成化合物。
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式_____________、_____________。
(2)右图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示___________,与每个“构成粒子”相邻的粒子呈______________空间构型。A与D按原子个数比l∶l形成的化合物的电子式为__________________。
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
|
化学键 |
F-D |
F-F |
B-B |
F-B |
C-D |
D-D |
|
键能/kJ·mol-1 |
460 |
176 |
347.7 |
347 |
745 |
497.3 |
①下列三种物质形成的晶体。熔点由高到低的顺序(用a、b、c表示):_________________
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②试估算F单质品体的燃烧热:_____________________________________
(1)NaHCO3 (1分)CH3COONa(1分)(或其它有机酸的盐)
(2)氢键(1分) 正四面体(1分) HOOH( 2分)
(3)①acb (2分)②990.7kJ/mol(2分)
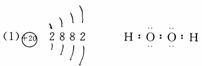 ⑵CH4
、 CO2、CS2
⑵CH4
、 CO2、CS2 CaC2+CO↑
CaC2+CO↑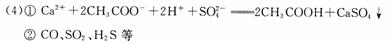
 1022
1022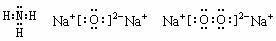 (共3分)氮化钠氢化钠也对
(共3分)氮化钠氢化钠也对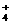 +OH―
+OH―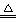 NH3↑+H2O (4分)
NH3↑+H2O (4分)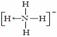 (→ ,表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
(→ ,表示共用电子对由N原子单方面提供),白磷(P4)的结构式为 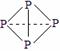 ,请画出N4H44+的结构式 。
,请画出N4H44+的结构式 。 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:__________________________________________。
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:__________________________________________。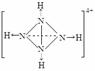 (3分)
(3分)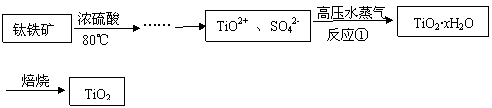
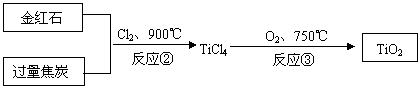
 TiO2·xH2O
+2H + (3分)
TiO2·xH2O
+2H + (3分)
 (2分)
(2分)