5.(10分)碱式氯化铝[Al2(OH)nCl6-n]m (1≤n≤6,m≤10) (商业代号BAC),是一种比Al2(SO4)3效果更好的净水药剂。以下是用煤矸石(主要含Al2O3,SiO2及少量铁的氧化物)为原料生产碱式氯化铝过程中遇到的情况:
(1)在反应器中加入16%的硫酸和16%的盐酸,在不断搅拌过程中再加入经过焙烧后的煤矸石粉,反应器上部有一条长管子作为反应时气体的排放管。加热至沸腾(102℃)并保持一段时间,期间不断用精密pH试纸在排气管口上方检查排出气体的pH,记录如下:
|
时间 |
起始 |
14min后 |
30min后 |
75min后 |
|
pH |
<2.0 |
=2.5 |
<3.5 |
=3.5 |
试解释排气管中放出气体的pH变化的原因________________________ __________
__ _如果把排气管加长一倍,排气的pH_________(回答“增大”“减小”或“不变化”),解释原因___________________________________________________________ _ ___
(2)上述反应结束后,冷却,过滤弃渣,然后再加热至100℃,并在不断搅拌的条件下,向溶液慢慢地添加Ca(OH)2至适量,生成大量沉淀。过滤上述溶液,弃渣,得到澄清的BAC稀溶液。将此稀溶液加热蒸发浓缩,又产生白色细晶状沉淀,经化验分析,知此沉淀不是BAC固体,也不是AlCl3晶体或Al(OH)3。问:这种物质是__________________,为什么此时会有沉淀析出________________________________________________ __
2.(10分)钛被称为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”。
(1)二氧化钛在现代社会里有广泛的用途,它的产量是一个国家国民经济发展程度的标志。我国至今产量不足,尚需进口二氧化钛。“硫酸法”生产二氧化钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质),主要生产流程是:
(1)将钛铁矿与浓H2SO4煮解: FeTiO3+2H2SO4(浓)===TiOSO4+FeSO4+2H2O
(硫酸钛酰)
|
(3)煅烧TiO2·nH2O===TiO2+nH2O
“硫酸法”生产TiO2排放的废液对水体有哪些污染,请指出主要的二点:
① ;
② 。
根据废液主要成分,针对其中一项污染,提出处理的方法。③
(2)某化学兴趣小组对Mg、Ti、Cu三种金属的金属活动性顺序进行探究。
提出假设:a. Ti金属活动性比Mg强;b. Ti金属活动性比Cu弱。
查阅资料:在相同条件下,金属与酸反应产生气泡的速度快,则该金属活动性越强。
实验设计:同温下,取大小相同的这三种金属薄片,用砂布将表面擦光亮,分别投入等体积等浓度的足量稀盐酸和稀HF溶液中反应,观察现象。
①稀盐酸:放出H2速率 Mg>Ti,铜不反应。 ②稀HF:放出H2速率 Ti>Mg
根据上述 现象(填①或②)得出金属活动性Mg Ti。如何解释另一反常现象 。
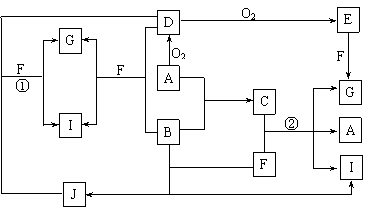
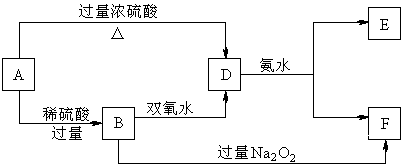
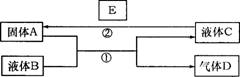 (1)若A是一种紫红色金属,气体D能
(1)若A是一种紫红色金属,气体D能 (10分)右图是一种常见有机物A的分子结构比例模型。
(10分)右图是一种常见有机物A的分子结构比例模型。 CH3CH2OH
CH2=CH2
CH3CH2OH
CH2=CH2 [CH2-CH2]n
[CH2-CH2]n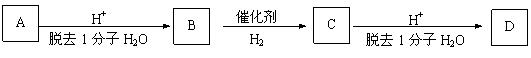
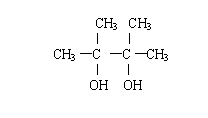 。
。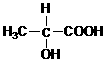 )就有旋光性。
)就有旋光性。