27.(10分)根据烷烃、烯烃、炔烃燃烧的反应式,有人总结出如下规律:
对于烷烃有:n(烷烃)= n(H2O)- n(CO2);对于烯烃: n(H2O)- n(CO2)= 0;对于炔烃有:n(炔烃)= n(CO2)- n(H2O)。请回答下列问题:
(1)C2H6和C2H4混合气1.0L在氧气中充分燃烧生成2.0LCO2和2.4L水蒸气(相同状况),则混合气中C2H6和C2H4的体积是 (填序号)。
(A)3:1 (B)1:3 (C)2:3 (D)3:2
(2)某混合气体由烯烃和烷烃或烯烃和炔烃组成。组成中可能是两种气体,也可能是多种气体。将1.0体积混合气在氧气中充分燃烧,产生3.0体积水蒸气和3.7体积CO2(相同状况下测定)。
①判断混合气由 和 两类烃组成。
②上述判断的理由是 (简要文字)。
③上述两类烃的体积比为 。
|
|
|
 例如:2CH3COOK + 2H2O CH3CH3
+ 2CO2↑ + H2↑ + 2KOH
例如:2CH3COOK + 2H2O CH3CH3
+ 2CO2↑ + H2↑ + 2KOH
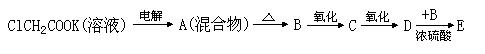 根据下列演变关系:
根据下列演变关系:
(1)写出电极反应式
阳极 ;阴极 。
(2)写出下列反应的化学方程式:

 A
B
; B C 。
A
B
; B C 。
(3)D和B在不同条件下反应,会生成3种不同的E,其中属于高分子的E为
。
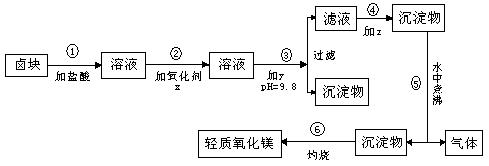
25.(9分)“卤块”的主要成分为MgCl2(含Fe3+、Fe2+、Mn2+等杂质离子),若以它为原料,按如下的工艺流程图,即可制得“轻质氧化镁”。
生成氢氧化物沉淀的pH 化学试剂价格表
|
物质 |
开始沉淀 |
沉淀完全 |
|
试剂 |
价格/元/吨 |
|
Fe(OH)3 |
2.7 |
3.7 |
漂液(含NaClO25.2%) |
450 |
|
|
Mn(OH)2 |
6.3 |
9.8 |
H2O2(30%) |
2400 |
|
|
Mg(OH)2 |
9.6 |
11.1 |
NaOH(固体,98%) |
2100 |
|
|
|
|
|
Na2CO3(固体99.5%) |
600 |
|
|
|
|
|
卤块(MgCl2,30%) |
310 |
如果要求产品尽量不含杂质,而且成本较低。请回答问题:
(1)在步骤②加入的氧化剂x,最佳选择应是 ,其作用是 。
(2)在步骤③加入的试剂y应是 ,之所以要控制pH=9.8,其目的
是 。
21. (6分)下列有关实验的叙述,正确的是(填序号)(少一个扣一分,多一个倒扣一分,扣完为止) 。
(A)配制500mL某物质的量浓度的溶液,可用两只250mL的容量瓶
(B)用渗析法分离淀粉中混有的NaCl杂质
(C)无法用分液漏斗将甘油和水的混合液体分离
(D)用酸式滴定管量取20.00mL高锰酸钾溶液
(E)为了测定某溶液的pH,将经水润湿的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
(F)用浓氨水洗涤做过银镜反应的试管
(G)配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
(H) 配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,应立即用滴管吸去多余的部分。
(J)在氢氧化铁胶体中加少量硫酸会产生沉淀
(K)用结晶法可以除去硝酸钾中混有的少量氯化钠
|
实验室制取Cl2的原理是:MnO2 + 4HCl(浓) === MnCl2 + 2H2O + Cl2↑
(1)从下图中挑选所需仪器,画出收集纯净干燥Cl2的装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。
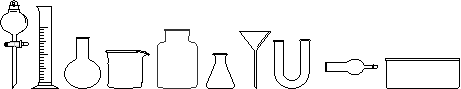
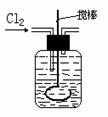 (2)将氯气通入盛有两种互不相溶的中性液体的容器中,如下图所示。当Cl2通入后,上层液体呈现棕色,且颜色由浅变深,然后用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(2)将氯气通入盛有两种互不相溶的中性液体的容器中,如下图所示。当Cl2通入后,上层液体呈现棕色,且颜色由浅变深,然后用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
① 上层液体通入Cl2后发生的
离子反应方程式是_____ ___。
②原上层液体是________________。
③原下层液体是________________。
④上下剧烈搅动的目的是____________________________。
⑤要检验上层液体中含有的金属离子,其方法是________,现象是_______。
⑥实验结束后,若要将两种液体分离,要用到的玻璃仪器是_______。
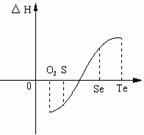 (2)等物质的量氧气、硫、硒、碲与H2反应的焓变
(2)等物质的量氧气、硫、硒、碲与H2反应的焓变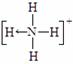 ⑶ 已知白磷、NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为
⑶ 已知白磷、NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为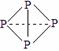
 NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:__________________________________________。
NH4++NH2-。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:__________________________________________。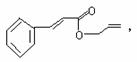 对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1-丙烯酯:
对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1-丙烯酯: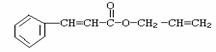
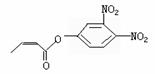 可简化为
可简化为