29.(13分)2005年诺贝尔化学奖授予在发现有机物合成转换方面作出杰出贡献的三名科学家:
法国的伊夫·肖万、美国的罗伯特·格拉布和理查德·施罗克。三位科学家获奖原因就是对有机化学烯烃复分解反应的研究作出贡献:他们弄清了如何指挥烯烃分子“交换舞伴”,将分子部件重新组合成别的物质。三人对于有机化学烯烃复分解反应的研究是通往“绿色化学”的重要一步。烯烃的复分解反应也称之为烯烃的歧化反应,反应机理可表示为:
|

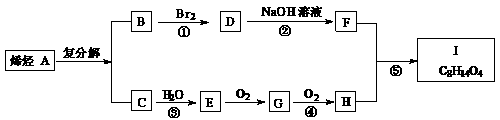
已知同温同压时,C相对于氢气的密度为14,I的分子式为C8H14O4,试根据下图关系,回答问题:
|
(1)已知C的燃烧热为Q kJ/mol,写出C完全燃烧的热化学方程式:
。
(2)反应①、②、③、④、⑤中,属于加成反应的是 。
(3)写出下列化合物的结构简式: A. , I. 。
(4)写出反应②的化学方程式: 。
(5)F有多种属于二元醇的同分异构体,除下列三种外,
|
 ,
,
写出其它同分异构体(一个碳原子上不能连接两个羟基)的结构简式:
。
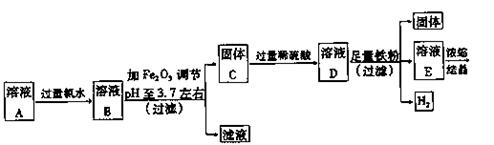
24.(15分)用硫酸处理铁悄所得到的溶液A中除Fe2+外,还含有一定量的Fe3+、Cu2+
|
实验1:制取硫酸亚铁晶体的过程如下图:
|
阳离子 |
开始沉淀的pH |
沉淀完全的pH |
|
Fe3+ |
2.7 |
3.7 |
|
Cu2+ |
5.4 |
6.9 |
|
Fe2+ |
8.1 |
9.6 |
|
Mn2+ |
8.3 |
9.8 |
(1)往溶液A中加过量氯水的作用是 。
(2)右表是使一些金属离子转化为氢氧化物沉淀的pH,根据表中数据分析,固体C是 。
(3)有人提出,在处理溶液B时,先加入几滴石蕊试液,然后逐滴加入NaOH溶液
|
你认为此方案是否可行? (填“行”或“不行”),
其理由是 。
实验2:用下图装置进行测定硫酸亚铁晶体(FeSO4·nH2O)中结晶水含量的实验(图中半透膜可让气体通过又可防止固体粉末进入导管):将m1g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水,冷却至常温后,称量玻璃管中固体的质量为m2g。
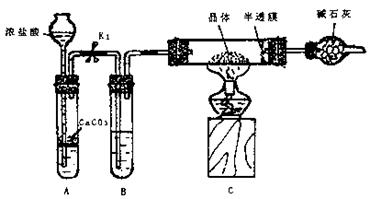
(1)B中的试剂是 。
(2)实验中有以下步骤:
①打开K1 ②关闭K1 ③点燃酒精灯 ④熄灭酒精灯火焰,使C中玻璃管冷却至常温。
正确的实验操作顺序是 (填以上选项序号)。
(3)根据实验结果,计算硫酸亚铁晶体中结晶水的n值为 。
(摩尔质量:FeSO4为152g·mol-1;H2O为18g·mol-1)



 惠南中学2007届高三第一学期期末考试
惠南中学2007届高三第一学期期末考试
 A.和浓硫酸混混合加热,可发生消去反应
A.和浓硫酸混混合加热,可发生消去反应