25.中学化学教材上有如下介绍:“在氢氧化钠浓溶液中加入氧化钙,加热,制成的白色固体就是碱石灰,它是水和二氧化碳的吸收剂”。有两个实验小组的同学决定通过实验探究碱石灰的组成。
(1)第一小组设计的实验方案如下
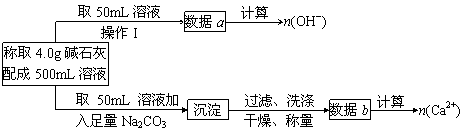

①下列关于溶液中n(OH-)、n(Ca2+)、n(Na+)之间的关系式正确的是_________(填序号)
A.n(Na+)+2n(Ca2+)= n(OH-)
B.2n(Na+)+n(Ca2+)=n(OH-)
C.n(Na+)+n(Ca2+)=2n(OH-)
②现有4.0g碱石灰,设其中n(Na+)=x mol,n(Ca2+)=y mol,请填写列空格:
|
碱石灰的可能组成 |
NaOH,CaO |
NaOH,CaO,Ca(OH)2 |
NaOH Ca(OH)2 |
NaOH, Ca(OH)2,H2O |
|
x、y之间关系式(等式或不等式) |
A |
40x+56y<4.0<40x+74y |
B |
C |
把表中A、B、C的关系式填在下面空格上:
A: ;B: ;C:
(2)第二小组查得如下资料:氢氧化钙在250℃时不分解,氢氧化钠在580℃时不分解。他们设计了如下方案并得出相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.6g,剩余固体在580℃时继续加热至恒重,固体质量又减少了0.7g 。请通过计算确定该碱石灰各成分的质量分数。
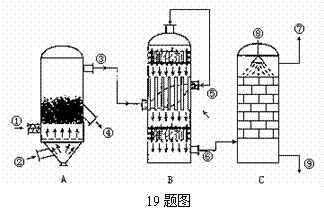
19.(共6分)
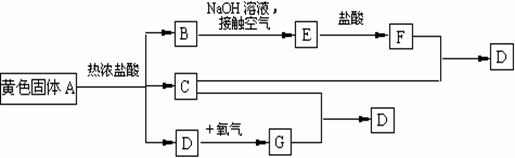
已知a、b、c、d、e分别是Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种物质水溶液中的各一种。它们互相反应的情况如下表所示:
|
|
a |
b |
c |
d |
e |
|
c |
↓ |
↓ |
╱ |
↑ |
- |
|
b |
↓ |
╱ |
↓ |
- |
- |
“↓”表示生成沉淀;“↑”表示产生气体;“-”表示无明显现象;“╱”表示实验未做。
则c 是 e是 (均填化学式)
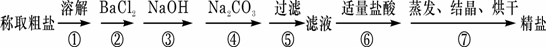
 (1)判断BaCl2已过量的方法是
(1)判断BaCl2已过量的方法是
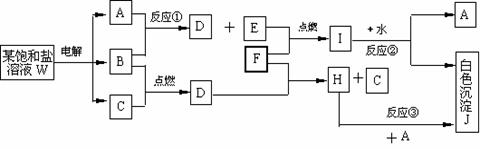

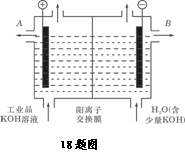 电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。