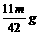2.20 g y x
x=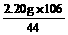 =5.30 g y=
=5.30 g y=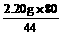 =4.00 g
=4.00 g
剩余固体NaOH的质量为:6.00 g-5.30 g=0.70 g
所以两种组成的质量分数分别为:
w
(Na2CO3)=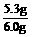 ×100%=88%
×100%=88%
w (NaOH)=100%-88%=12%
NaOH溶液的质量分数为: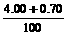 ×100%=4.7%
×100%=4.7%
答案: (1) 第一份的固体组成:w (Na2CO3)=77%,w (NaHCO3)=23%;第二份固体组成w (Na2CO3) =88%,w (NaOH)=12%
(2) 第一份NaOH溶液的质量分数为3.5%,第二份NaOH溶液的质量分数为4.7%
 例题2-23
例题2-23
 如图2-7所示,用来验证绿色植物进行光合作用的实验装置,先将这个装置放在暗室里24 h,然后移到阳光下;瓶子内盛有NaOH溶液,瓶口密封。
如图2-7所示,用来验证绿色植物进行光合作用的实验装置,先将这个装置放在暗室里24 h,然后移到阳光下;瓶子内盛有NaOH溶液,瓶口密封。
(1)经过相当长的一段时间以后,摘下植物的叶片,经过处理后加碘液数滴而叶片颜色无变化,证明液片中__________,说明了__________。
(2)瓶内放NaOH的作用是_____;将绿色植物放置24 h的作用是_____________。
(3)若瓶内析出m g白色沉淀,说明_____,发生反应的化学方程式为__________,将此沉淀加热,可得到多少克CO2气体?
 解析与答案
解析与答案
叶片经处理后加碘液不变色,说明叶片中无淀粉。淀粉遇碘变蓝,这是淀粉的特性。
此时淀粉已被消耗,考虑光合作用的暗反应过程,CO2固定和还原均需要酶参与催化,这个过程消耗了淀粉。
|
2NaHCO3=Na2CO3+CO2↑+H2O。
答案: (1) 无淀粉; CO2是光合作用的原料。
(2) 吸收CO2;消耗植物体内原有淀粉。
|
2NaHCO3=Na2CO3+H2O+CO2↑
2×84 44
m g x
x=