摘要:( )由下列实验不能得出的相应结论的是 A.将燃着的木条伸入集气瓶中.木条停止燃烧.则集气瓶中盛放的是二氧化碳 B.将带火星的木条伸入集气瓶中.木条复燃.说明氧气已经集满 C.在甲烷燃烧的火焰上罩一干而冷的烧杯.烧杯内壁出现水珠.说明甲烷的成分中含有氢 D.给气体加压.气体的体积缩小.说明气体分子之间有间隙
网址:http://m.1010jiajiao.com/timu3_id_91758[举报]
(2012?宁德质检)实验台上分类摆放下列药品,兴趣小组欲利用这些药品进行铝和铜性质的探究.

Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的
(3)比较铝和铜的金属活动性强弱,可选用上述的
[提出问题]该气体是什么呢?
[猜想]甲同学认为可能是氧气;乙同学认为可能是氢气;丙同学认为可能是二氧化硫.
[探究实验]闻该气体的气味,发现没有气味,排除了
对余下两种气体猜想进行如下实验:
[思维拓展]由以上探究实验可以推知,硫酸铜溶液中有
查看习题详情和答案>>

Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
B
B
.A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的
氧化铝保护膜
氧化铝保护膜
.该变化的化学方程式为4Al+3O2
2Al2O3
| ||
4Al+3O2
2Al2O3
.
| ||
(3)比较铝和铜的金属活动性强弱,可选用上述的
①⑤⑥或③⑤
①⑤⑥或③⑤
(填序号)试剂进行实验.Ⅱ.将铝片插入硫酸铜溶液中,一段时间后取出,铝片上没有明显变化,其原因是铝片表面未用砂纸进行打磨,清除氧化膜
铝片表面未用砂纸进行打磨,清除氧化膜
.兴趣小组把处理过的铝片放入硫酸铜溶液中,除铝片上有红色金属析出外,还发现有较多气泡产生,于是激发了他们的探究欲望.[提出问题]该气体是什么呢?
[猜想]甲同学认为可能是氧气;乙同学认为可能是氢气;丙同学认为可能是二氧化硫.
[探究实验]闻该气体的气味,发现没有气味,排除了
丙
丙
同学的猜想.对余下两种气体猜想进行如下实验:
| 实验步骤 | 现象 | 结论 |
收集一试管气体, 收集一试管气体, 用带火星木条检验 用带火星木条检验 |
木条不复燃 | 该气体不是氧气 |
| 收集一试管气体,用拇指堵住管口,移近酒精灯火焰 | 发出轻微的爆鸣声,并产生淡蓝色火焰 | 该气体是 氢气 氢气 |
氢
氢
离子参与反应.
夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.

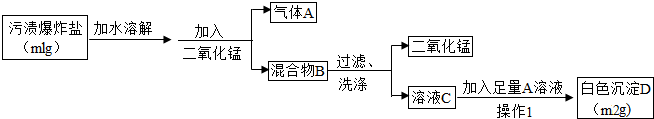
查阅相关资料:“污渍爆炸盐”主要有效成份为过碳酸钠,化学式为2Na2CO3?3H2O2,俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
探究一:确证污渍爆炸盐的化学成分及其化学式
小强同学的实验设计如下所示.请你运用初中所学知识,帮助小强同学完成下列探究.
(1)小强同学把带火星的木条伸入气体A中,带火星的木条复燃,则气体A为 ,说明“污渍爆炸盐”溶于水生成过氧化氢;
(2)小强从氢氧化钙溶液和氢氧化钡溶液这两种溶液中选择氢氧化钡溶液作为加入的A溶液,则小强选择的理由为 ;
实验过程中观察到 ,说明“污渍爆炸盐”溶于水生成碳酸钠;
(3)操作Ⅰ为 、洗涤、干燥,检验沉淀是否洗涤干净的方法是 ;
实验的初步结论
小强认为:“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,“污渍爆炸盐”的主要化学成分是过碳酸钠.
(4)若m1=31.4,m2=39.4,请根据数据计算确证污渍爆炸盐的化学式为2Na2CO3?3H2O2.
计算过程:解:
探究二:变质污渍爆炸盐的纯度测定
已知:过碳酸钠与硫酸溶液反应的化学方程式如下:
2Na2CO3?3H2O2+2H2SO4=2Na2SO4+3H2O2+2CO2↑+2H2O 2H2O2
2H2O+O2↑
为测定已变质的过碳酸钠(污渍爆炸盐部分变质后的成分为2Na2CO3?3H2O2和Na2CO3)的纯度,设计如图所示的实验:Q为-具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中.
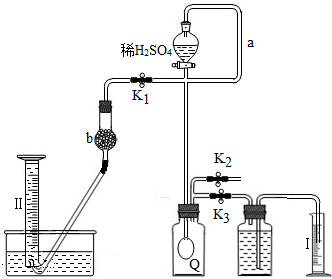
(1)Q内发生反应生成的气体为 .在样品中加入少量二氧化锰的目的是 .导管a作用是 .
(2)为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭 (填K1、K2或K3,下同).打开 .
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是 ,b中装的碱石灰的作用是 ,为何要缓缓打开K1的理由是 .
(4)实验结束时,量筒I中有123.4mL水,量筒Ⅱ中收集到33.6mL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是 (保留小数点后一位;标准状况下气体的密度:CO2-1.96g/L,O2-1.43g/L).
(5)某同学实验测得的过碳酸钠的纯度偏大,你认为可能的原因是 .
A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ
B.量筒Ⅱ读数时,量筒液面高于水槽液面
C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x
D.气体体积数值x、y没有扣除滴加的硫酸的体积. 查看习题详情和答案>>


查阅相关资料:“污渍爆炸盐”主要有效成份为过碳酸钠,化学式为2Na2CO3?3H2O2,俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
探究一:确证污渍爆炸盐的化学成分及其化学式
小强同学的实验设计如下所示.请你运用初中所学知识,帮助小强同学完成下列探究.
(1)小强同学把带火星的木条伸入气体A中,带火星的木条复燃,则气体A为
(2)小强从氢氧化钙溶液和氢氧化钡溶液这两种溶液中选择氢氧化钡溶液作为加入的A溶液,则小强选择的理由为
实验过程中观察到
(3)操作Ⅰ为
实验的初步结论
小强认为:“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,“污渍爆炸盐”的主要化学成分是过碳酸钠.
(4)若m1=31.4,m2=39.4,请根据数据计算确证污渍爆炸盐的化学式为2Na2CO3?3H2O2.
计算过程:解:
探究二:变质污渍爆炸盐的纯度测定
已知:过碳酸钠与硫酸溶液反应的化学方程式如下:
2Na2CO3?3H2O2+2H2SO4=2Na2SO4+3H2O2+2CO2↑+2H2O 2H2O2
| ||
为测定已变质的过碳酸钠(污渍爆炸盐部分变质后的成分为2Na2CO3?3H2O2和Na2CO3)的纯度,设计如图所示的实验:Q为-具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中.

(1)Q内发生反应生成的气体为
(2)为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是
(4)实验结束时,量筒I中有123.4mL水,量筒Ⅱ中收集到33.6mL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是
(5)某同学实验测得的过碳酸钠的纯度偏大,你认为可能的原因是
A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ
B.量筒Ⅱ读数时,量筒液面高于水槽液面
C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x
D.气体体积数值x、y没有扣除滴加的硫酸的体积. 查看习题详情和答案>>
 3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:
3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:(一)水--常用的化学试剂
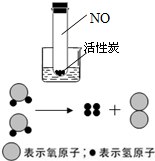
(1)为验证活性炭的吸附能力和温度的关系,某同学将底部装有活性炭颗粒、充满红棕色NO2气体(有毒气体)的试管插入盛有水的烧杯中(如图),然后向烧杯中加入NH4NO3,观察到试管中红棕色慢慢变淡至褪色,说明
温度越低,活性炭的吸附能力越好
温度越低,活性炭的吸附能力越好
;(2)电解水时,需在水中加入少量氢氧化钠或硫酸,目的是
为了增强水的导电性
为了增强水的导电性
,如图是实验室电解水的微观示意图,其中最小的微粒是原子
原子
,通过该实验可以得出的结论是水是由氢元素和氧元素组成的
水是由氢元素和氧元素组成的
.(二)海水--人类的资源宝库
(1)获取淡水:将海水转化为淡水,最常用的操作方法是
蒸馏法
蒸馏法
;(2)获取NaCl:将海水进行
蒸发
蒸发
可得到粗盐;为除去粗盐中含有的Na2SO4、CaCl2等杂质,可依次进行下列操作:①溶解;②加过量的BaCl2溶液; ③加过量的Na2CO3溶液;④过滤;⑤加适量的X溶液;⑥蒸发结晶.其中适量X溶液是稀盐酸
稀盐酸
(填名称);(3)提取金属镁:海水中含有丰富的镁元素,如图是从海水中提取镁的简单流程:
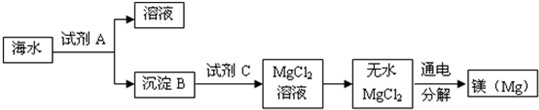
上述流程中,沉淀B是Mg(OH)2,则试剂A可以用
氢氧化钙
氢氧化钙
溶液,试剂C的化学式为HCl
HCl
,由无水MgCl2制取Mg的化学方程式为MgCl2
Mg+Cl2↑
| ||
MgCl2
Mg+Cl2↑
,属于
| ||
分解
分解
反应.(三)清洁卫生的水--人类需要
(1)保护运河,我提建议:①生活污水处理后排放;②将工厂废液排入运河;③使用无磷洗衣粉,④减少燃放烟花爆竹 ⑤及时清理运河中疯长的藻类.你认为以上建议中可以采纳的是
①③④⑤
①③④⑤
(填序号);(2)以下是污水处理成自来水的工艺流程示意图:
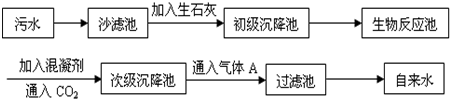
①污水中含Ca2+、Mg2+、HCO3-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,初级沉降池中生成的主要沉淀是
碳酸钙
碳酸钙
和碳酸镁
碳酸镁
;(MgCO3微溶于水)②通入CO2除了能调节自来水的pH,还能
除去过量的氢氧化钙
除去过量的氢氧化钙
;③生物反应池是利用微生物直接分解水中的有机物,以除去水中过多的氮、磷等有害成分.这样做的优点是
不会产生污染,比较环保
不会产生污染,比较环保
;④工艺中的混凝剂常用
明矾
明矾
,其除去悬浮固体小颗粒的过程A
A
;(填编号)A.只是物理过程 B.只是化学过程 C.是物理和化学过程
⑤气体A是
Cl2
Cl2
(填化学式),其作用是杀菌消毒,使自来水符合卫生标准;⑥俗话说:“大灾之后必有大疫”,这主要是因为灾民饮用了含有大量的细菌和杂质的水后,很容易患肠道传染病.请你设计合理方案,将被污染的水处理成能饮用的水:
加入明矾净水、然后过滤、用氯气杀菌消毒、最后加热煮沸
加入明矾净水、然后过滤、用氯气杀菌消毒、最后加热煮沸
.实验台上分类摆放下列药品,兴趣小组欲利用这些药品进行铝和铜性质的探究。
① ② ③ ④ ⑤ ⑥
② Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的 。该变化的化学方程式为
(3)比较铝和铜的金属活动性强弱,可选用上述的 (填序号)试剂进行实验。Ⅱ.将铝片插入硫酸铜溶液中,一段时间后取出,铝片上没有明显变化,其原因是 。
兴趣小组把处理过的铝片放入硫酸铜溶液中,除铝片上有红色金属析出外,还发现有较多气泡产生,于是激发了他们的探究欲望。
【提出问题】该气体是什么呢?
【猜 想】甲同学认为可能是氧气
乙同学认为可能是氢气
丙同学认为可能是二氧化硫
【探究实验】闻该气体的气味,发现没有气味,排除了 同学的猜想。
对余下两种气体猜想进行如下实验:
| 实验步骤 | 现象 | 结论 |
| | 木条不复燃 | 该气体不是氧气 |
| 收集一试管气体,用拇指堵住管口,移近酒精灯火焰 | 发出轻微的爆鸣声,并产生淡蓝色火焰 | 该气体是 |
实验台上分类摆放下列药品,兴趣小组欲利用这些药品进行铝和铜性质的探究。

① ② ③ ④ ⑤ ⑥
② Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的 。该变化的化学方程式为
(3)比较铝和铜的金属活动性强弱,可选用上述的 (填序号)试剂进行实验。Ⅱ.将铝片插入硫酸铜溶液中,一段时间后取出,铝片上没有明显变化,其原因是 。
兴趣小组把处理过的铝片放入硫酸铜溶液中,除铝片上有红色金属析出外,还发现有较多气泡产生,于是激发了他们的探究欲望。
【提出问题】该气体是什么呢?
【猜 想】甲同学认为可能是氧气
乙同学认为可能是氢气
丙同学认为可能是二氧化硫
【探究实验】闻该气体的气味,发现没有气味,排除了 同学的猜想。
对余下两种气体猜想进行如下实验:
【思维拓展】由以上探究实验可以推知,硫酸铜溶液中有 离子参与反应.

① ② ③ ④ ⑤ ⑥
② Ⅰ.(1)铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关
A.铝在地壳中含量高 B.铝相对活泼,冶炼较难 C.铝的硬度小
(2)铝制品具有很好的抗腐蚀性能,是因为铝在空气中其表面易形成致密的 。该变化的化学方程式为
(3)比较铝和铜的金属活动性强弱,可选用上述的 (填序号)试剂进行实验。Ⅱ.将铝片插入硫酸铜溶液中,一段时间后取出,铝片上没有明显变化,其原因是 。
兴趣小组把处理过的铝片放入硫酸铜溶液中,除铝片上有红色金属析出外,还发现有较多气泡产生,于是激发了他们的探究欲望。
【提出问题】该气体是什么呢?
【猜 想】甲同学认为可能是氧气
乙同学认为可能是氢气
丙同学认为可能是二氧化硫
【探究实验】闻该气体的气味,发现没有气味,排除了 同学的猜想。
对余下两种气体猜想进行如下实验:
| 实验步骤 | 现象 | 结论 |
| | 木条不复燃 | 该气体不是氧气 |
| 收集一试管气体,用拇指堵住管口,移近酒精灯火焰 | 发出轻微的爆鸣声,并产生淡蓝色火焰 | 该气体是 |