摘要: 如右图所示是元素周期表的一部分.关于元素X.Y.Z的叙述正确的是( ) ①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐 ②Y.Z的气态氢化物的水溶液的酸性:Y<Z ③Z的单质在常温下是液体.可与铁粉反应 ④Z的原子序数比Y大19 ⑤Z所在的周期中含有32种元素 A.①②③④ B.①②③④⑤ C.只有③ D.①④ [解析] 从题中各元素在周期表中所处的位置.得出该图为元素周期表右上角的一部分.由此可以依次判断出各元素:R为He.X为N.Y为S.Z为Br.X的气态氢化物为NH3.而Y的最高价氧化物对应的水化物为H2SO4.它们可反应生成硫酸铵.①正确,Y.Z的气态氢化物分别为H2S.HBr.HBr的水溶液为强酸.H2S的水溶液为弱酸.故②正确,说法③符合客观事实.正确,Z的原子序数为35.而Y的原子序数为16.④正确,Z所在周期为第四周期.从19号元素开始.到36号元素结束.共18种元素.⑤错误.综上所述.正确的答案为A. [答案] A
网址:http://m.1010jiajiao.com/timu3_id_87013[举报]
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
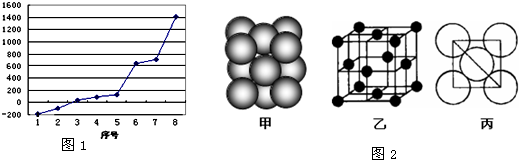
试回答下列问题:
(1)请写出字母O代表的元素符号
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
(4)k与l形成的化合物kl2的电子式是
 ,它在常温下呈液态,形成晶体时,属于
,它在常温下呈液态,形成晶体时,属于
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为
(用M、NA、d表示).
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式
查看习题详情和答案>>
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | ||||||||||||||||

试回答下列问题:
(1)请写出字母O代表的元素符号
Fe
Fe
,该元素在周期表中的位置第四周期第 VIII族
第四周期第 VIII族
.(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表
Si
Si
(填元素符号);其中电负性最大的是2
2
(填如图1中的序号).(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
SiC
SiC
(填化学式),试从结构角度加以解释:因SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
因SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
.(4)k与l形成的化合物kl2的电子式是


分子
分子
晶体.(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为
4
4
,该晶体的密度_
| ||
| 8NAd3 |
| ||
| 8NAd3 |
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式
NH4++Al3++5OH-+2SO42-+2Ba2+=NH3↑+3H2O+AlO2-+2BaSO4↓
NH4++Al3++5OH-+2SO42-+2Ba2+=NH3↑+3H2O+AlO2-+2BaSO4↓
. 下表是元素周期表的一部分.表中所列的编号分别代表一种化学元素.
下表是元素周期表的一部分.表中所列的编号分别代表一种化学元素.| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑩ | ⑧ | ⑨ | |||||||||||||||
(1)请写出⑨代表的元素基态原子电子排布式
1s22s22p63s23p63d84s2
1s22s22p63s23p63d84s2
.(2)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”代表
Si
Si
(填元素符号);其中电负性最大的是Cl
Cl
(填元素符号).(3)由⑤原子跟②原子以1:1相互交替结合而形成的晶体,其晶型与②对应的一种晶体相同.两者相比熔点更高的是
金刚石
金刚石
(填中文名称),原因是:同为原子晶体,但金刚石晶体中C-C键长短于碳化硅晶体中的Si-C键长,故金刚石熔点更高
同为原子晶体,但金刚石晶体中C-C键长短于碳化硅晶体中的Si-C键长,故金刚石熔点更高
.(4)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3?6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
| 2 |
| 3 |
试推断紫色晶体的化学式为
[Ti(H2O)6]Cl3
[Ti(H2O)6]Cl3
.如图所示是元素周期表中第一、第二周期10种元素的某些性质的一组数据(所列数据的单位相同),除带“…”的四种元素外,其余元素都给出了该种元素的全部该类数据.
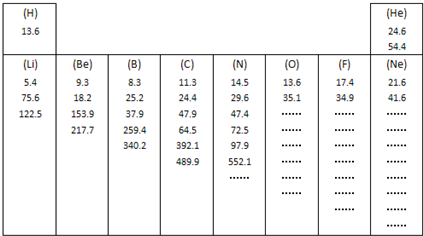
研究这些数据,回答下列问题:
(1)每组数据可能是该元素的 (填序号);
A.原子得到电子所放出的能量 B.原子半径的大小
C.原子逐个失去电子所吸收的能量 D.原子及形成不同分子的半径的大小
(2)分析同周期自左向右各元素的第一个数据:
①总体变化趋势是 (填“增大”或“减小”);
②与前后元素相比,由于该元素的数值增大较多而变得反常的元素位于元素周期表的 族;
③根据你分析所得的变化规律推测,镁和铝的第一个数据的大小关系为Mg(1) Al(1)(填“大于”或“小于”).
(3)分析每个元素的一组数据:
①有些元素的一组数据中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中 的结论.
②根据这个规律,你认为氧元素8个数据中出现“突跃”的数据应该是第 个.
查看习题详情和答案>>

研究这些数据,回答下列问题:
(1)每组数据可能是该元素的
A.原子得到电子所放出的能量 B.原子半径的大小
C.原子逐个失去电子所吸收的能量 D.原子及形成不同分子的半径的大小
(2)分析同周期自左向右各元素的第一个数据:
①总体变化趋势是
②与前后元素相比,由于该元素的数值增大较多而变得反常的元素位于元素周期表的
③根据你分析所得的变化规律推测,镁和铝的第一个数据的大小关系为Mg(1)
(3)分析每个元素的一组数据:
①有些元素的一组数据中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中
②根据这个规律,你认为氧元素8个数据中出现“突跃”的数据应该是第
如表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
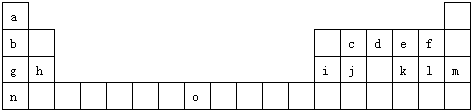
试回答下列问题:
(1)请写出元素O的基态原子电子排布式 .
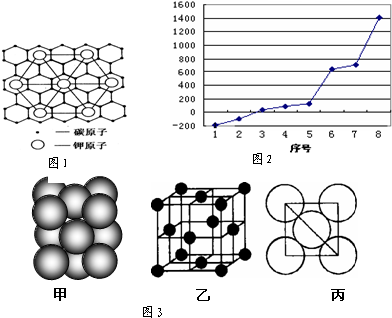
(2)c元素的一种同素异形体与熔融的n单质形成石墨间隙化合物,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见图1,则x值为 .
(3)第三周期8种元素按单质熔点高低的顺序如图2,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号).
(4)由i原子跟d原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.则i与d形成的晶体中一个晶胞中含有4个i原子;与同一个i原子相连的d原子构成的空间构型为 ,d原子的杂化类型为 .
(5)i单质晶体中原子的堆积方式如图3甲所示,其晶胞特征如图3乙所示,原子之间相互位置关系的平面图如图3丙所示.若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,则该晶体的密度为 _g/cm3 (用字母表示).
查看习题详情和答案>>

试回答下列问题:

(1)请写出元素O的基态原子电子排布式
(2)c元素的一种同素异形体与熔融的n单质形成石墨间隙化合物,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见图1,则x值为
(3)第三周期8种元素按单质熔点高低的顺序如图2,其中序号“8”代表
(4)由i原子跟d原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.则i与d形成的晶体中一个晶胞中含有4个i原子;与同一个i原子相连的d原子构成的空间构型为
(5)i单质晶体中原子的堆积方式如图3甲所示,其晶胞特征如图3乙所示,原子之间相互位置关系的平面图如图3丙所示.若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,则该晶体的密度为
(13分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素,试回答下列问题:
| A |
| R | |||||||||||||||
| B |
|
|
|
|
|
|
|
|
|
|
| C | D | E | F | T | |
| G | H | I | J |
| K | L |
| ||||||||||
|
|
|
|
|
| M |
| N |
|
|
|
|
|
|
|
|
|
|
(1)请写出G的淡黄色化合物与二氧化碳反应的方程式 。
(2)D的气态氢化物的VSEPR模型为 _ ,其中心原子的杂化类型为___ _ _ _ _ 。
(3)G、H和I的第一电离能数值由大到小的顺序为: (用元素符号作答)。
(4)由A、C、D形成的1mol ACD分子中,含有 个σ键, 个π键。
(5)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的
元素还有_______________(填元素符号),其中一种金属的晶胞结构如右
图所示,该晶胞中含有金属原子的数目为 。
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2
是__________(填“极性”或“非极性”)分子。
③在C2H4、CH3Cl、CH2O、CS2、CCl4五种有机化合物中,碳原子采取sp2杂化的分子有____________(填分子式)。
查看习题详情和答案>>