摘要:15.高锰酸钾是锰的重要化合物和常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.请回答下列问题: (1)通常高锰酸钾保存在棕色试剂瓶中.下列试剂不需要用棕色试剂瓶保存的是 . a.浓硝酸 b.氯水 c.烧碱溶液 (2)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列物质不同的是 . a.84消毒液 b.75%酒精 c.臭氧 d.双氧水 (3)写出MnO2催化H2O2溶液制氧气的化学方程式 . (4)①通常状况下.酸性高锰酸钾溶液不能与下列物质中的 反应. a.乙醇 b.Na2SO3溶液 c.环己烯 d.苯 e.FeSO4溶液 ②将用稀硫酸酸化的高锰酸钾溶液滴入盛有足量草酸溶液的试管中.振荡后.观察到的现象是 .已知1 mol草酸参加反应时转移的电子数是2×6.02×1023.锰元素在生成物中的化合价为+2.请写出此反应的化学方程式为 . 解析:(1)浓硝酸和氯水见光均会分解.故需要保存在棕色试剂瓶中. (2)高锰酸钾的消毒机理是利用它的强氧化性.84消毒液.臭氧.双氧水用于消毒均是利用它们的强氧化性. (3)双氧水分解制备氧气的化学方程式为:2H2O2MnO22H2O+O2↑. (4)①酸性高锰酸钾溶液可与乙醇.Na2SO3溶液.环己烯.FeSO4溶液发生氧化还原反应.只与苯不反应.故选d,②草酸与酸性高锰酸钾溶液发生氧化还原反应使高锰酸钾溶液的紫色褪去,根据反应中1 mol草酸转移电子的物质的量为2 mol.用电子守恒配平得化学方程式为:2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+10CO2↑+8H2O. 答案:b (3)2H2O22H2O+O2↑ (4)①d ②高锰酸钾溶液的紫色褪去 2KMnO4+5H2C2O4+3H2SO4===2MnSO4+K2SO4+10CO2↑+8H2O
网址:http://m.1010jiajiao.com/timu3_id_86638[举报]
必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
mol KMnO4.
查看习题详情和答案>>

(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与下列
BD
BD
(填序号)物质相似.A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
2MnO2+4KOH+O2
2K2MnO4+2H2O
| ||
2MnO2+4KOH+O2
2K2MnO4+2H2O
.
| ||
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
K2MnO4
K2MnO4
.(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
KOH
KOH
和MnO2
MnO2
(写化学式).(5)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |
(1)化学实验必须注意安全,下列做法存在安全隐患的是
A.氢气还原氧化铜实验中,先加热氧化铜后通氢气
B.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拨开橡皮塞并投入碎瓷片
C.实验室做钠的实验时,余下的钠屑投入到废液缸中
D.配制浓硫酸与酒精混合液时,将1体积的酒精倒入3体积的浓硫酸中
E.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
F.制乙烯时,用量程为300℃的温度计代替量程为200℃的温度计,测反应液的温度
(2)工业制备高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.

①KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是
a、84消毒液(NaClO溶液) b、双氧水 c、苯酚 d、75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是
a、浓硝酸 b、硝酸银 c、氯水 d、烧碱
③上述流程中可以循环使用的物质有
④若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
mol KMnO4.
⑤该生产中需要纯净的CO2气体.若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)
a、石灰石 b、稀HCl c、稀H2SO4 d、纯碱
⑥操作Ⅰ的名称是
查看习题详情和答案>>
ABCD
ABCD
(选填序号).A.氢气还原氧化铜实验中,先加热氧化铜后通氢气
B.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拨开橡皮塞并投入碎瓷片
C.实验室做钠的实验时,余下的钠屑投入到废液缸中
D.配制浓硫酸与酒精混合液时,将1体积的酒精倒入3体积的浓硫酸中
E.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
F.制乙烯时,用量程为300℃的温度计代替量程为200℃的温度计,测反应液的温度
(2)工业制备高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.

①KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是
ab
ab
(填代号).a、84消毒液(NaClO溶液) b、双氧水 c、苯酚 d、75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是
d
d
(填代号).a、浓硝酸 b、硝酸银 c、氯水 d、烧碱
③上述流程中可以循环使用的物质有
MnO2
MnO2
、KOH
KOH
(写化学式).④若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |
⑤该生产中需要纯净的CO2气体.若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)
cd
cd
.a、石灰石 b、稀HCl c、稀H2SO4 d、纯碱
⑥操作Ⅰ的名称是
过滤
过滤
;操作Ⅱ根据KMnO4和K2CO3两物质在溶解度
溶解度
(填性质)上的差异,采用浓缩结晶
浓缩结晶
(填操作步骤)、趁热过滤得到KMnO4粗晶体.高锰酸钾是锰的重要化合物和常用的氧化剂.如图所示是工业上用软锰矿制备高锰酸钾的一种工艺流程.

(1)KMnO4稀溶液是一种常用的消毒剂,其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.双氧水 c.福尔马林(35%甲醛溶液) d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶中,下列试剂保存不需要棕色试剂瓶的是
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有
(4)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
或0.67mol
或0.67molmol KMnO4.
(5)写出实验室用KMnO4制备气体的一个化学方程式
(6)操作Ⅰ的名称是
查看习题详情和答案>>

(1)KMnO4稀溶液是一种常用的消毒剂,其消毒原理与下列物质相同的是
ab
ab
(填代号).a.84消毒液(NaClO溶液) b.双氧水 c.福尔马林(35%甲醛溶液) d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶中,下列试剂保存不需要棕色试剂瓶的是
d
d
(填代号).a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有
MnO2
MnO2
、KOH
KOH
(写化学式).(4)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |
(5)写出实验室用KMnO4制备气体的一个化学方程式
2KMnO4
K2MnO4+MnO2+O2↑;
| ||
2KMnO4
K2MnO4+MnO2+O2↑;
| ||
(6)操作Ⅰ的名称是
过滤
过滤
;操作Ⅱ根据KMnO4和K2CO3两物质在溶解度上的差异(溶解度数据:K2CO3 20℃时为112g,100℃时为156g;KMnO4 20℃时为6.4g,100℃时为30g)采用浓缩结晶
浓缩结晶
(填操作步骤)、趁热过滤的方法得到KMnO4粗晶体.(2013?武清区三模)高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿(主要成分MnO2)制备高锰酸钾的一种工艺流程.

请回答:
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与
a.NaClO溶液 b.乙醛 c.双氧水 d.75%的酒精
(2)操作Ⅰ的名称是
(3)上述流程中可以循环使用的物质有
mol KMnO4.
(4)MnO2在酸性条件下具有强氧化性,可被还原为Mn2+.写出MnO2与浓盐酸制取氯气的化学方程式
为验证MnO2具有强氧化性,下列方案可行的是
A.MnO2固体加入到FeCl3溶液中,再加KSCN溶液,观察溶液是否变红
B.MnO2固体加入到Na2SO3溶液中,再加BaCl2溶液,观察是否有白色沉淀生成
C.MnO2固体加入到FeSO4与KSCN的酸性混合液中,观察溶液是否变红
(5)酸性KMnO4与H2C2O4溶液反应,反应开始时溶液褪色较慢,反应一段时间后褪色会迅速加快,其原因是
查看习题详情和答案>>

请回答:
(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与
ac
ac
(填字母)相同.a.NaClO溶液 b.乙醛 c.双氧水 d.75%的酒精
(2)操作Ⅰ的名称是
过滤
过滤
;硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
(3)上述流程中可以循环使用的物质有
KOH
KOH
和MnO2
MnO2
(填化学式).若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得| 2 |
| 3 |
| 2 |
| 3 |
(4)MnO2在酸性条件下具有强氧化性,可被还原为Mn2+.写出MnO2与浓盐酸制取氯气的化学方程式
MnO2+4HCl(浓)
MnCl2+Cl2 ↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2 ↑+2H2O
| ||
为验证MnO2具有强氧化性,下列方案可行的是
C
C
(填字母)A.MnO2固体加入到FeCl3溶液中,再加KSCN溶液,观察溶液是否变红
B.MnO2固体加入到Na2SO3溶液中,再加BaCl2溶液,观察是否有白色沉淀生成
C.MnO2固体加入到FeSO4与KSCN的酸性混合液中,观察溶液是否变红
(5)酸性KMnO4与H2C2O4溶液反应,反应开始时溶液褪色较慢,反应一段时间后褪色会迅速加快,其原因是
反应生成的Mn2+,起催化作用
反应生成的Mn2+,起催化作用
.工业上制备的高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
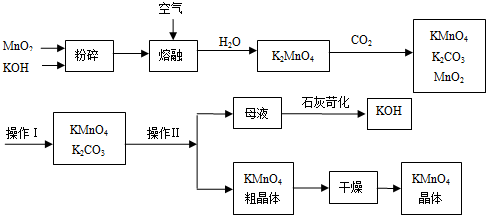
①KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
③上述流程中可以循环使用的物质有、(写化学式)
④若不考虑物质循环与制备过程中的损失,则1molMnO2
可制得molKMnO4.
⑤该生产中需要纯净的CO2气体.若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)
a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱.
查看习题详情和答案>>

①KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是
ab
ab
(填代号).a.84消毒液(NaClO溶液) b.双氧水 c.苯酚 d.75%酒精
②高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是
d
d
(填代号).a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
③上述流程中可以循环使用的物质有、(写化学式)
MnO2、KOH
MnO2、KOH
.④若不考虑物质循环与制备过程中的损失,则1molMnO2
| 2 |
| 3 |
| 2 |
| 3 |
⑤该生产中需要纯净的CO2气体.若实验室要制备纯净的CO2,所需试剂最好选择(选填代号)
cd
cd
.a.石灰石 b.稀HCl c.稀H2SO4 d.纯碱.