摘要:某密闭容器中充入等物质的量的气体A和B.在一定压强和温度下发生反应:A(g)+xB.达到平衡后.只改变反应的一个条件.测得容器中物质的浓度.反应速率随时间的变化如下图所示.下列说法中正确的是( ) A.30 min时降低温度.40 min时升高温度 B. 0-8 min内A的平均反应速率为0.08 mol·L-1·min-1 C. 反应方程式中的x=1.正反应为吸热反应 D. 54 min时C的体积分数大于40 min时 解析:根据时间-浓度变化图.20 min时反应达到平衡.此时A.B浓度减小1 mol·L-1.C的浓度为2 mol·L-1.推知x=1.则有:A.根据时间-速率图象.30 min时.正.逆反应速率降低.但平衡没有移动.不可能是降低温度引起的.可能是减小压强.40 min时改变条件导致正.逆反应速率均增大.但40 min瞬间A.B.C的浓度均不变.故改变的条件是升高温度.又因为逆反应速率增大的倍数大于正反应.平衡向逆反应方向移动.故54 min达到平衡时.C的体积分数小于40 min时.且推知反应为放热反应.0-8 min内.Δc(A)=2.0 mol·L-1-1.36 mol·L-1=0.64 mol·L-1.Δt=8 min.故v(A)=0.08 mol·L-1·min-1.综合上述.选项B正确. 答案:B
网址:http://m.1010jiajiao.com/timu3_id_85261[举报]
一定温度下,某密闭容器中充入等物质的量的气体A和B,发生如下反应:A(g)+xB(g)?2C(g).达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如下图所示.请回答下列问题:

(1)该反应的化学平衡常数表达式为K=
(x要算出具体的数字).在该条件下,当v(B)正:v(C)逆=
(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是
(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
则:C1、C2、C3三者数值的关系式为
查看习题详情和答案>>

(1)该反应的化学平衡常数表达式为K=
| c2(C) |
| c(A)×c(B) |
| c2(C) |
| c(A)×c(B) |
1:2
1:2
时反应达到了化学平衡状态.(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是
K2=K1
K2=K1
.(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |
C3=2C1=2C2
C3=2C1=2C2
(用代数式表示)某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法中正确是( )
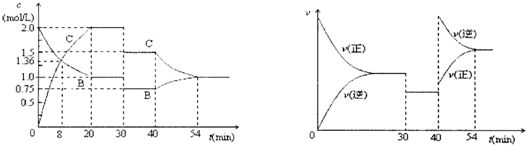

| A、8min时表示正反应速率等于逆反应速率 | B、前20min A的反应速率为1.00mol/(L?min ) | C、反应方程式中的x=1,30min时表示增大压强 | D、40min时改变的条件是升高温度,且正反应为放热反应 |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应是:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示.下列说法中正确是( )

查看习题详情和答案>>
 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示.下列说法中正确是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示.下列说法中正确是( )
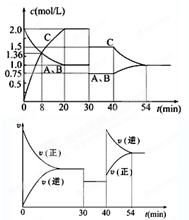 某密闭容器中充入等物质的量A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法正确的是( )
某密闭容器中充入等物质的量A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法正确的是( )